下列实验能证明一元酸HA是弱电解质的是
| A.将25℃ 1mL pH=3的HA溶液加水稀释至100mL,稀释后溶液的PH=4 |
| B.HA溶液与NaHCO3溶液反应放出CO2 |
| C.25℃时,NaA溶液的pH大于7 |
| D.往HA溶液中滴入甲基橙,溶液呈橙色,不呈红色。 |
下列反应中,硫元素表现出氧化性的是
| A.稀硫酸与锌粒反应 | B.二氧化硫与氧气反应 |
| C.浓硫酸与碳反应 | D.三氧化硫与水反应 |
ClO2是新一代饮用水的消毒剂,许多发达国家的自来水厂采用ClO2代替Cl2来进行自来水消毒。我国最近成功研制出制取ClO2的新方法,其反应的微观过程如下所示: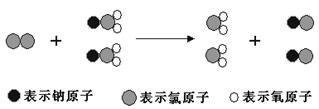
下列有关该反应的叙述中正确的是
| A.该反应是复分解反应 |
| B.该反应的化学方程式为Cl2+2NaClO2=2ClO2+2NaCl |
| C.反应中Cl2既是氧化剂,又是还原剂 |
| D.NaClO2和ClO2中Cl的化合价相同 |
小明家中有如下生活用品:碘酒、食盐、食醋、84消毒液(有效成分为NaClO),小明利用上述用品不能完成的任务是
| A.检验买来的奶粉中是否加有淀粉 | B.检验自来水中是否含有Cl- |
| C.除去保温瓶中的水垢 | D.洗去白色衣服上的番茄汁 |
C、N、S的氧化物中许多是工业上重要的化工原料,但是当它们分散到空气中时,会带来很多环境问题。下列有关这些元素的氧化物说法错误的是
A.开发太阳能、水能、风能、氢能等新能源将有利于减少这些元素的氧化物的产生
B.N与S的某些氧化物能直接危害人的身体健康,引发呼吸道疾病
C.“温室效应”与二氧化碳的排放有着直接的关系
D.这些氧化物使雨水的pH<7,我们把pH<7的雨水称之为酸雨
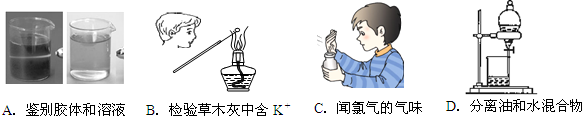
下图所示的实验操作,不能达到相应目的的是