下列各原子或离子的电子排布式错误的是
| A.Na+: 1s22s22p6 | B.F :1s22s22p5 |
| C.O2--: 1s22s22p4 | D.Ar: 1s22s22p63s23p6 |
100mL 0.1 mol·L-1醋酸与50mL 0.2 mol·L-1氢氧化钠溶液混合,在所得溶液中
| A.C(Na+)>C(CH3COO-)>C(OH-)>C(H+) |
| B.C(Na+)>C(CH3COO-)>C(H+)>C(OH-) |
| C.C(Na+)>C(CH3COO-)>C(H+)=C(OH-) |
| D.C(Na+)=C(CH3COO-)>C(OH-)>C(H+) |
25 ℃时,水的电离达到平衡:H2O H++OH-;△H>0,下列叙述正确的是
H++OH-;△H>0,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,KW增大,pH不变 |
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH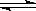 CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
在一定温度下的密闭容器中,当下列物理量不再变化时,表明A(s) +2B(g)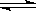 C(g)+ D(g)已达到平衡的是
C(g)+ D(g)已达到平衡的是
| A.混合气体的压强 | B.混合气体的分子数目 |
| C.混合气体的密度 | D.混合气体的总物质的量 |
微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-===ZnO+H2O;Ag2O+H2O+2e-===2Ag+2OH-根据上述反应式,判断下列叙述中正确的是
| A.在使用过程中,电池负极区溶液的pH减小 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Ag2O是负极,Zn是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |