①MgCl2 ②干冰③冰 ④Na2O2 ⑤白磷(P4)⑥硫磺 ⑦Na2CO3 ⑧金刚石 ⑨NaOH ⑩SiO2
(1)以上物质中属于离子晶体的是 ;
(2)属于分子晶体的是 。
(3)属于原子晶体的是_________(填序号)
将镁铝的混合物0.1mol溶于100ml 2mol/L硫酸溶液中,然后再滴加1mol/L的NaOH溶液,请回答:
(1)若在滴加NaOH溶液过程中,沉淀质量随加入NaOH溶液的体积变化如图所示,当V1=160mL时,则金属粉末中n(Mg)=mol, V2=mL,
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积 V(NaOH) =mL
V(NaOH) =mL
(3)图像中A点的意义是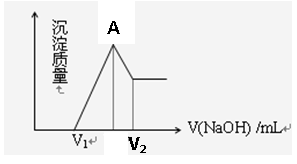
已知在含HNO3的溶液中放入Al不生成H2。某无色透明溶液跟金属铝反应放出H2。试判断下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO32-、SO42-、HCO3-、OH-、NO3-,在下列两种情况下何者能存在于溶液中。
(1)当生成Al3+时,可能大量存在_________________________________________________。
(2)当生成 时,可能大量存在_______________________________________________。
时,可能大量存在_______________________________________________。
取两等份铝粉,第一份加入250 mL 2 mol·L-1的盐酸,第二份加入400 mL2mol·L-1的烧碱。若同温同压下放出气体体积之比为5:6,则加入的铝粉每份质量为。
(10分) 将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如右图所示。当V1=140mL时,则金属粉末中n(Mg)= mol,V2= mL。
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) mL。
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入480 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:
(4)若滴加NaOH溶液致V2ml时,停止滴加NaOH溶液,开始往溶液中通入足量CO2,请写出发生反应的离子方程式——————————————————————-————。
(9分)有一透明溶液,可能含有Al3+、Fe3+、K+、Mg2+和Cu2+、 CO32-、SO42-等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。而且加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
试推断:
(1)原溶液中一定含有——————————;
(2)一定不含有————————————————;
(3)可能含有————————;为了进一步确定可能含有的离子,请简述实验操作过程—————————————————————————。