(11分)工业上制备BaCl2的工艺流程图如图7:
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。
已知:BaSO4(s) + 4C(s) 4CO(g) + BaS(s) △H1 =" +571.2" kJ·mol-1 ①
4CO(g) + BaS(s) △H1 =" +571.2" kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2=" +226.2" kJ·mol-1 ②
2CO2(g) + BaS(s) △H2=" +226.2" kJ·mol-1 ②
(1)高温焙烧时常把原料粉碎,目的是_________________________________
(2)常温下,相同浓度的Na2S和NaHS溶液中,说法正确的是: (3分)
| A.Na2S溶液的pH比NaHS溶液pH大 |
| B.两溶液中含有的离子种类不同 |
| C.两溶液中滴入同体积同浓度的盐酸,产生气体速率相等 |
| D.两溶液中加入NaOH固体,c(S2-)都增大 |
E. NaHS溶液中:c(Na+) > c(HS-)> c(OH-) > c(H+) > c(S2-)
(3)反应C(s) + CO2(g) 2CO(g)的△H =
2CO(g)的△H =
(4)制备BaCl2的工艺流程图中气体A用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为:
(5)实际生产中必须加入过量的炭,同时还要通入空气,目的是:
(写出一种原因即可)
一定量的铁粉在氯气中充分燃烧后,将所得固体完全溶于稀盐酸,制得溶液A。
(1)铁在氯气中燃烧的化学方程式是__________________________。
(2)推测A中可能含有的金属阳离子:①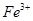 ;②只有
;②只有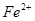 ;③_____________。
;③_____________。
甲同学为探究溶液的组成,实验如下:
| 实验步骤 |
实验现象 |
实验结论及反应离子方程式 |
| 取少量溶液A于试管中,加入KSCN溶液 |
_____________ |
假设②不成立,假设①或③成立;反应的离子方程式是___。 |
(3)乙同学继续探究溶液A的组成。
查阅资料: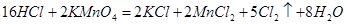
实验过程:另取少量溶液A于试管中,逐滴加入酸性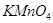 溶液,充分振荡,
溶液,充分振荡,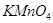 紫色褪去。
紫色褪去。
实验结论:_____________(填字母序号)。
a. 可能有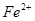 b. 可能无
b. 可能无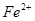 c. 一定有
c. 一定有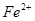
下表为元素周期表的一部分,参照元素①~⑧在表中的位置,用化学用语 回答下列问题:
回答下列问题: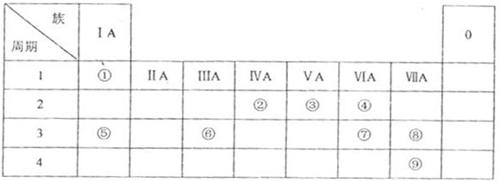
(1)④、⑤、⑦形成的简单离子的半径由大到小的顺序是____________________。
(2)含 ⑦的最高价氧化物对应水化物的稀溶液与足量⑤的最高价氧化物对应水化物的稀溶液反应放出热量
⑦的最高价氧化物对应水化物的稀溶液与足量⑤的最高价氧化物对应水化物的稀溶液反应放出热量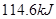 ,此反应的热化学方程式为____________________。
,此反应的热化学方程式为____________________。
(3)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为______________________________。
N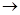 ⑥的单质的化学方程式为________________________________________。
⑥的单质的化学方程式为________________________________________。
M溶液中离子浓度由大到小的顺序为________________________________________。
(4)设计实验探究⑧、⑨两种元素非金属性的相对强弱。
可选用的试剂有:氯水、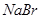 溶液、
溶液、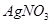 溶液、
溶液、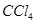 。
。
请完成实验 报告单:
报告单:
| 实验内容 |
现象 |
步骤一:试管1:取少量氯水:试管2:取少量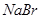 溶液,滴加少量氯水。 溶液,滴加少量氯水。 |
试管2中的现象是:____________________ |
| 步骤二:分别向试管1、试管2中加入试剂________,振荡。 |
试管2中的现象是_________________ |
| ①试管1的作用是________________________________。 ②实验结论是____________________________________________,产生该结论的原因是:同主族元素从上到下________,得电子能力逐渐减弱。 |
I. 现有下列8种物质
① ;②
;② ;③
;③ ;④HF;⑤
;④HF;⑤ ;⑥
;⑥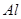 ;⑦食盐水;⑧
;⑦食盐水;⑧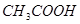
其中属于强电解质的是_____________(填序号,下同),既能跟盐酸反应又能跟 溶液反应的是_____________。
溶液反应的是_____________。
II. 现有一瓶浓度为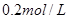 的某酸溶液,可能为醋酸、盐酸、硫酸中的一种,为了确定该酸溶液的组成进行实验:取
的某酸溶液,可能为醋酸、盐酸、硫酸中的一种,为了确定该酸溶液的组成进行实验:取 该酸
该酸 溶液,逐滴加入
溶液,逐滴加入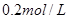 的氢氧化钠溶液,恰好反应完全时所需碱液体积为
的氢氧化钠溶液,恰好反应完全时所需碱液体积为 ,请用化学用语回答:
,请用化学用语回答:
(1)该酸不可能是____________;
(2)用pH试纸测得反应后所得溶液呈碱性,根据此现象说明该酸溶液为____________,用离子方程式说明溶液呈碱性的原因_________ _______________。
_______________。
III. A、B、C、D均为可溶于水的固体,组成它们的离子有:
| 阳离子 |
 、 、 、 、 、 、 |
| 阴离子 |
 、 、 、 、 、 、 |
分别取它们的水溶液进行实验,结果 如下:
如下:
①A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会消失。
②C与D反应有红褐色沉淀生成并放出气体。
③B与C反应有白色沉淀生成并放出气体。
(1)写出它们的化学式:A___________,B___________,C___________,D___________。
(2)写出③中B与C反应的离子方程式_________________________________。
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________。
A. KMnO4 B. H2O2 C. Cl2水 D. HNO3
然后再加入适当物质 调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。
调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8. 0×10-38,Cu(OH
0×10-38,Cu(OH )2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀
)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀 完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶
完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶 液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”)。
液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”)。
(12分 )在2L密闭容器中,800℃时反应2NO(g)+O2(g)
)在2L密闭容器中,800℃时反应2NO(g)+O2(g)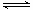 2NO2(g)体系中,n(NO)
2NO2(g)体系中,n(NO) 随时间的变化如表:
随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=___________________。
已知:K(300℃)>K(350℃),该反应是________热反应。
(2)图 中表示NO2的变化曲线是____________。用O2表示从0~2s内该反应的平均速率v=___________。
中表示NO2的变化曲线是____________。用O2表示从0~2s内该反应的平均速率v=___________。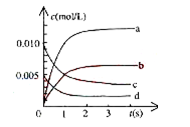
(3)能说明该反应已经达到平衡状态的是___________。
a、v(NO2)=2v(O2) b、容器内压强保持不变
c、v逆(NO)=2v正(O 2) d、容器内的密度保持不变
2) d、容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a、及时分离出NO2气体 b、适当升高温度
c、增大O2的浓度 d、选择高效的催化剂