当前,校车生产及安全问题再次引发社会强烈关注。为了防止校车事故频频发生,2012年3月29日国务院召开常务会议,审议并原则通过《校车安全管理条例(草案)》。
Ⅰ.安全性是校车的一项重要的指标。
(1)在某次校车碰撞实验中出现了下列现象,其中属于化学变化的是( )
| A.玻璃破碎 | B.轮胎爆炸 | C.车子变形 | D.油箱着火 E.安全气囊打开 |
Ⅱ.校车生产中用到的材料
(2)铁、铜、铝是校车生产中常用的金属材料。
①请设计实验证明三种金属的活动性顺序。
②铝在常温下有较强的抗腐蚀能力的原因是 。
若校车生产中需要1 t铝,则需要含氧化铝90%的铝土矿多少吨?(2Al2O3 4Al + 3O2↑)
4Al + 3O2↑)
③钢铁材料在焊接前,首先要进行除锈,此时发生的化学反应方程式为 。钢铁防锈常用方法有 (至少二项)。
(3)橡胶、塑料、锦纶、皮革等也是校车生产中常用的材料。
①橡胶、塑料及锦纶均属于 材料。
②鉴别羊毛、锦纶的方法是 。
Ⅲ.校车的燃料。
(4)汽油、柴油、乙醇、天然气都可以用于汽车燃料,但随着油价的不断攀升,后者开始备受青睐。请写出上述任一种燃料燃烧的化学方程式。
请根据下列实验装置图回答有关问题: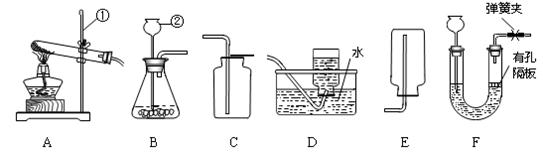
(1)请写出标号仪器的名称:①,②。
(2)实验室选用B、D装置制取O2,反应的化学方程式是;
(3)选择发生装置B和收集装置(选填序号)可用于实验室制取较为干燥的CO2,对应的化学方程式是;若将发生装置由B改为F,其优点是。若将收集装置改用下图G所示医用塑料袋,则气体导入端为(填“a”或“b”)。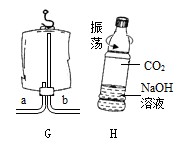
(4)用上图H所示的矿泉水瓶进行对比实验,可以证明CO2与NaOH溶液确实发生了反应,应做的对比试验是。
化学与我们的身体健康和生产生活有着密切的关系。
(1)下列食物中富含蛋白质的是(填序号)。
A.大米 B.瘦肉 C.菠菜
(2)水是人及一切生物生存所必需的,电解水可证明水由氢、氧两种元素组成,该反应的化学方程式为。
(3)到目前为止,人类使用的燃料主要是煤、和天然气等化石燃料,其中天然气的主要成分为。
现有八种物质,选择相应物质的字母填空:
A纯碱 B武德合金 C硝酸钾 D过磷酸钙
E.石墨 F.熟石灰 G.生石灰 H.干冰
(1)可用作复合肥料; (2)可用作食品干燥剂;
(3)可制作保险丝;(4)可用作电极。
(5)可用作配制波尔多液; (6)可作制冷剂。
以下是我们日常生活中常用各种清洗剂。
| 名称 |
洗涤灵 |
洁厕灵 |
炉具清洁剂 |
活氧彩漂 |
污渍爆炸盐 |
| 产品样式 |
 |
 |
 |
 |
 |
| 有效成分 或功能 |
清洗油污 |
盐酸 |
氢氧化钠 |
过氧化氢 |
过碳酸钠 |
(1)我们使用洗涤灵清洗餐具上的油污,这是因为它具有的功能。
(2)清除以下物质,可以使用洁厕灵的是填字母序号)。
A.铁锈 B.水垢(主要成分为碳酸钙和氢氧化镁)
C.油渍 D.氢气还原氧化铜实验后,试管内壁残留的红色固体
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,这一反应了体现右图中(选填①②③④)性质关系。
(4)将洁厕灵滴入炉具清洁剂中,如图甲所示。
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外) ;此时溶液可用图乙中点处(选填A、B、C)表示。
②若反应后溶液pH为7,图丙中a微粒的化学式为。
(5)①“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是(填序号)。
②氧化氢溶液常用于医用消毒,某兴趣小组为测定一瓶久置的医用过氧化氢溶液中溶质质量分数。他们取该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。试计算该过氧化氢溶液中溶质的质量分数。
(写出计算过程)
金属在生产生活中应用广泛。
(1)下图是铝的原子结构示意图。下列说法不正确的是。
A.铝原子的质子数为13 B.化合物中铝元素通常显+3价
C.铝是地壳中含量最多的元素 D.铝可作导线是由于它具有良好的导电性
(2)21世纪是钛的世纪。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程: 
①反应Ⅰ在800~900 ℃的条件下进行,还生成一种可燃性无色气体,该反应的化学方程式为___ __;
②反应II可获得海锦钛,化学方程式表示为TiCl2+2Mg高温Ti+2MgCl2。该反应属于
(填序号)。
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
③该工艺流程中,可循环利用的两种物质是、。
(3)现有铝、铁、铜、银四种金属相互转化关系如图所示。 试推理乙是;写出甲→丙反应的化学方程式。
(4)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是 。
A.a点溶液中的溶质有4种
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段溶液,滴加稀盐酸,有白色沉淀
D.取d点的固体,加入稀盐酸,有气泡产生
(5)相同质量的锌、铁分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是。