4分)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,这引起了同学们的兴趣。难道生成的硫酸铜粉末受热后还能分解?那分解的产物是什么呢?
通过查阅资料,同学们了解到:
A.硫酸铜受热分解生成氧化铜和气体。气体是由SO2、SO3、O2中的一种或几种。受热时温度不同,生成的气体成分也不同。
B.SO2、SO3都能被碱石灰吸收。
C.SO2、SO3都能被氢氧化钠溶液吸收。
【提出猜想】根据质量守恒定律猜测气体的成分:
I. 只含 __ 一种; II.含有SO2、O2二种; III.含有SO2、SO3、O2三种。
【设计实验】利用下图装置加热硫酸铜粉末直至完全分解 
A B C D
【获取事实】
(1)用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有 __ 。
(2)已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
| 装置 |
A(试管+粉末) |
B |
C |
| 反应前 |
42.0克 |
75.0克 |
140.0克 |
| 反应后 |
37.0克 |
79.5克 |
140.0克 |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个 ? __
A.3CuSO43CuO+SO3↑+2SO2↑+O2↑ B. 4CuSO44CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO45CuO+SO3↑+4SO2↑+2O2 ↑ D. 6CuSO46CuO+4SO3↑+2SO2↑+O2↑
实验室用98%的浓硫酸配制稀硫酸,并进行相关的性质实验。(夹持仪器省略,装置气密性良好)
(1)配制100g19.6%的稀硫酸的步骤是Ⅰ.;Ⅱ.量取;Ⅲ.溶解。读取水的体积时,视线应与量筒内液体保持水平。
(2)与金属反应实验:锌粒与稀硫酸反应制取氢气
AB CDE
仪器a的名称是,锌粒与稀硫酸反应的化学方程式是。以上五个装置不可能收集到氢气的是(填写字母编号)。比较B、C装置,B装置的优点是。能随时控制反应进行或停止,符合该条件的发生装置是。
(3)鉴别实验:现需鉴别三包失去标签的白色固体,它们可能是碳酸钙、氯化钡、硝酸钾,请
按下表完成实验设计:
| 步骤一: (物理方法) |
取样于三支试管中分别加入 试剂。 |
现象: |
先鉴别出碳酸钙固体 |
| 步骤二: (化学方法) |
再任取一支未鉴别出试剂的试管中滴入稀硫酸 |
现象: |
小明在做实验时发现实验室中有一瓶标签受损的无色液体,如图所示。小明的化学兴趣小组对此产生了疑问。
【提出问题】这瓶无色液体是什么呢?
【做出猜想】根据初中所学的化学知识,该液体只能是
过氧化氢溶液、碳酸、稀硫酸和蒸馏水中的一种。
【讨论交流】 大家讨论后一致认为
(1)不可能是蒸馏水,理由是。
(2)不可能是碳酸,理由是碳酸不稳定,易分解。
【实验验证】
为确定该液体成分,同学们继续进行了如下实验探究:
| 实验操作 |
实验现象 |
实验结论 |
| 步骤一: 取该液体适量于试管中,向其中加入少量粉末 |
没有气泡产生。 |
该液体不是过氧化氢溶液。 |
| 步骤二: 取该液体适量于试管中,向其中滴加少量氯化钡溶液。 |
该液体是稀硫酸。 |
【反思交流】
(1)大家认为标签受损的原因可能是 。
(2)如果该液体是过氧化氢溶液,请用化学方程式表示步骤一中所发生的化学反应:。
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
提出问题:这瓶试剂可能是什么溶液呢?
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是
A.酸 B.碱 C.盐
查阅资料:Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性。
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
| 溶解度g |
36 |
109 |
215 |
9.6 |
得出结论:小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是。
设计实验并继续探究:
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是。
(2)小强为了确定该溶液是哪种溶液,他又进行了如下实验:
| 操作步骤 |
实验现象 |
结论及化学方程式 |
| 取样于试管中,滴加 |
产生大量的气泡 |
该溶液是 |
拓展与应用:确定该溶液还可以选择与小强不同的试剂,你选择的试剂是(要求类别不同)。
钢铁是人类生活和生产中非常重要的材料。
(3)工业炼铁的反应过程如下图所示,其中焦炭的作用是燃烧提供能量和。
(4)在工业冶炼中要得到224t,理论上需要含Fe2O380%,的赤铁矿石的质量是多少?
验证某混合气体含有CO和H2,并除去含有的少量CO2杂质。甲同学进行了如下实验: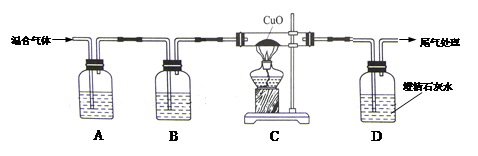
(1)A中氢氧化钠溶液的作用是,B中浓硫酸的作用是吸收水分,观察到C中黑色氧化铜变,D中澄清石灰水变浑浊,写出D中反应的化学方程式 。
(2)乙同学认为上述实验现象不能确定混合气体含有H2,他改进实验后证明了混合气体中含有H2。请写出乙同学的实验改进方法和现象。从环境保护角度,该实验中最后导出的尾气处理方法是。
(3)丙同学对A装置反应后的溶液成分进行验证,请根据实验现象填写下列空白处:
| 实验操作过程 |
实验现象 |
实验结论 |
| Ⅰ.取待测液少量于试管中,向其中滴加适量溶液 |
产生白色沉淀 |
溶液中含Na2CO3 |
| Ⅱ.将上述反应后的混合物静置后,再向上层清液中加入溶液。 |
溶液呈红色 |
溶液中含NaOH |
若将Ⅱ中加入的溶液换成(写化学式),也可得出Ⅱ中相同的结论。
写出相应的化学方程式为:。
根据下图四个化学实验,回答问题:(提示:Cu与Zn的合金称为黄铜)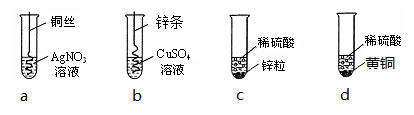
(1)描述实验a中的实验现象。
(2)要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是(填实验序号)。
(3)在c实验后的剩余溶液中,一定有的溶质是,可能有的溶质是,为了确定可能有的溶质,可加入(填选项序号)
Ⅰ.氯化钡溶液Ⅱ.氢氧化铜Ⅲ.氢氧化钠溶液Ⅳ.锌粒
(4)为了测定d中稀硫酸的溶质质量分数,取20g该黄铜样品于烧杯中,向其中分4次加入该稀硫酸,充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
| 加入稀硫酸的质量(g) |
充分反应后剩余固体的质量(g) |
|
| 第1次 |
25 |
16.75 |
| 第2次 |
25 |
13.5 |
| 第3次 |
25 |
m |
| 第4次 |
25 |
12.0 |
试回答下列问题:
Ⅰ.上述表格中m的值为;
Ⅱ.该稀硫酸的溶质质量分数是多少?(根据化学方程式计算)