验证某混合气体含有CO和H2,并除去含有的少量CO2杂质。甲同学进行了如下实验: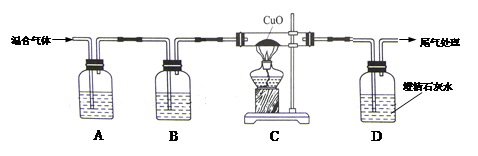
(1)A中氢氧化钠溶液的作用是 ,B中浓硫酸的作用是吸收水分,观察到C中黑色氧化铜变 ,D中澄清石灰水变浑浊,写出D中反应的化学方程式 。
(2)乙同学认为上述实验现象不能确定混合气体含有H2,他改进实验后证明了混合气体中含有H2。请写出乙同学的实验改进方法和现象 。从环境保护角度,该实验中最后导出的尾气处理方法是 。
(3)丙同学对A装置反应后的溶液成分进行验证,请根据实验现象填写下列空白处:
| 实验操作过程 |
实验现象 |
实验结论 |
| Ⅰ.取待测液少量于试管中,向其中滴加适量 溶液 |
产生白色沉淀 |
溶液中含Na2CO3 |
| Ⅱ.将上述反应后的混合物静置后,再向上层清液中加入 溶液。 |
溶液呈红色 |
溶液中含NaOH |
若将Ⅱ中加入的溶液换成 (写化学式),也可得出Ⅱ中相同的结论。
写出相应的化学方程式为: 。
(本题的所有夹持仪器均已省略)请根据下图回答问题: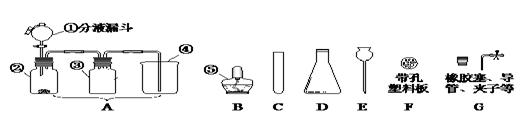
(1)图中仪器④⑤的名称④,⑤。
(2)实验室制取氧气,某同学设计了图A的装置,并用仪器③收集氧气。其中,仪器①中盛放的试剂应为,此法生成氧气的化学方程式为,
如果用排水法收集氧气,请补充完整A中集气瓶中的导管。
(3)实验室制取二氧化碳,从B~G中选择仪器,组装发生装置,要求能方便控制反应的发生或停止,你的正确选择为(填字母),反应的化学方程式为。
(4)实验室通常用如右图所示的洗气装置可用于检验二氧化碳气体,洗气瓶里面填装的药品可以是:(填字母)。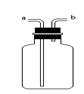
A.澄清石灰水 B.紫色石蕊溶液 C.水
有关反应的化学方程式为。
(5)如选用右图装置来收集CO2,则气体应从端(填“a”或“b”)进入。
(一)学习了二氧化碳性质后,某课外活动小组为了探究二氧化硫(SO2)的某些性质,进行了以下探究实验:下图中从左向右依次是某同学做的实验及相应现象。
(1)通过上述实验,小明同学可得二氧化硫气体的二点性质,分别是:
①;
②;
(2)A操作中,导气管要尽量接近试管底部,其目的是。
(二)酒精灯的灯焰分三个部分,为了探究灯焰的温度,科研人员用特殊的测温装置进行实验,结果如下:
| 外焰温度 |
内焰温度 |
焰心温度 |
| 840 |
896 |
686 |
①根据上表数据,灯焰三部分温度由低到高的顺序为;
②根据上表数据,加热实验时,被加热的仪器或物品应该放置在位置较适宜。
③实验中,若燃着的酒精灯中酒精不足,现要添加酒精,采取的操作是:先;再向酒精灯中添加酒精。
我会实验
根据图完成下列各题。( 共18分,每空2分)
A BC D E
郭大志同学欲探究氧气的性质,他用过氧化氢为原料制取并收集几瓶氧气。请回答下列问题
(1).实验室用过氧化氢制取氧气可选用和装置连接制取和收集氧气。
(2).郭大志同学收集了一瓶氧气用来做铁丝燃烧的实验,结果看不到火星四射的现象,其原因可能的是(任写一点)。经过排查,实验成功了,请写出铁丝燃烧的化学反应表达式(用化学式或文字表示均可),
(3).A装置漏斗下端管口插到液面下,是为了防止。C、E装置中的导管末端均接近集气瓶底部,其目的是。
(4).实验室用加热固体醋酸钠和碱石灰粉末的方法制备甲烷气体(密度比空气小,难溶于水),可选用和装置连接制取和收集甲烷。张光标同学在制取甲烷气体的过程中,发现试管破裂了,其原因可能是(写一点)
我会探究 ( 共10分,每空2分)
请你参与下面的实验探究,把下列表格和横线的空白处填写完整。
(1)提出问题:陈胜同学用“双氧水”(过氧化氢)清洗伤口时,不小心将过氧化氢溶液滴到水泥地板上,发现有大量的气泡产生。陈胜联想到自己曾用二氧化锰做过氧化氢的催化剂。他想,水泥块是否也可以做过氧化氢分解的催化剂呢?于是他到附近的建筑工地取回一些水泥块,并用蒸馏水浸泡、冲洗、干燥,并进行了以下的实验探究。
(2)猜想:水泥块能做过氧化氢的催化剂。
(3)实验验证:
| 实验步骤 |
实验现象 |
实验结论 |
|
| 实验一 |
木条不复燃 |
常温下过氧化氢溶液不分解 |
|
| 实验二 |
在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 |
木条复燃 |
(4)结论:水泥块能加快过氧化氢的分解速率,故水泥块能做过氧化氢分解的催化剂。
(5)讨论与反思:张山认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,她觉得需要增加一个探究实验,探究。
该实验步骤如下:
A、准确称量水泥块的质量;B、完成实验二;C、待反应结束后,将实验二试管的物质进行过滤 、洗涤 、干燥、。D、对比反应前后水泥块的质量。
分析:如果水泥块反应前后质量不变,则说明水泥块可以做过氧化氢分解的催化剂。
(6)李朋认为,要证明陈胜的猜想,张山的补充实验还不够,还需要再补充一个探究实验,探究。
在学校的国庆联欢会上,某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小军对此很感兴趣,于是,进行探究。
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想] ① 可能有一种气体和另一种物质生成
② 反应过程中可能有能量变化
[设计装置]如图所示
[实验探究]
实验一:探究反应后生成的气体是什么?
⑴ 打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是。
⑵ 实验中,还观察到伸入烧杯中的导管口有气泡冒出,
请解释产生该现象的原因:;
实验二:继续探究反应后生成的另一种物质是什么?
⑴ 小张猜想另一种物质是Na2CO3,小军认为不可能。
小军的依据是:;
为了证实小军的看法,请你帮助设计一个证明Na2CO3不存在的实验。从资料中查阅知道:Na2CO3与稀盐酸反应会产生二氧化碳。
| 实验步骤 |
实验现象 |
实验结论 |
| 向反应后试管中的剩余物加适量的稀盐酸,并将可能产生的 气体通入澄清石灰水中 |
若__________________ 实验中无此现象 |
说明__________________ 说明__________________ |
⑵ 小军从资料中查阅知道:若向含有OH—的溶液中滴入无色酚酞试液,就会出现红色。于是他取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的剩余物中含有(写物质名称或化学式)。
[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式:。