实验室用下图装置制取少量溴苯,试填写下列空白。
①向三颈烧瓶中加入苯和液溴的混合物,观察到三颈烧瓶和锥形瓶中出现的现象:______________________________。反应的化学方程式:_____________________。
②反应结束后,三颈烧瓶底部出现:______________________________________。
③锥形瓶内导管没有伸入水面以下的目的:___________________________
④干燥管中碱石灰的作用:_____________。
实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
(1)溶解时
(2)过滤时
(3)蒸发时
可用于分离或提纯物质的方法有:①过滤②蒸馏③加热④分液(填序号)
(1)除去石灰水中悬浮的CaCO3颗粒
(2)除去NaCl晶体中混有的碘单质
(3)分离石油中各不同沸点范围的成分
(4)分离水和苯的混合物
(11分) “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题: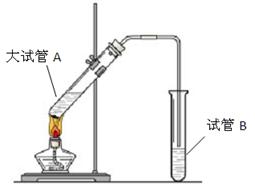
(1)写出制取乙酸乙酯的化学反应方程式:
(2)试管B中盛放的溶液是,其主要作用是
。
(3)装置中通蒸气的导管不能插入试管B的溶液中,目的是 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(5)做此实验时,往往还向大试管A中加入几块碎瓷片,其目的是 。
(6)用30g乙酸与46g乙醇反应,如果实际产量是理论产量的67%,则实际得到乙酸乙酯的质量是 。
| A.44g | B.29.5g | C.74.8g | D.88g |
图2是研究甲烷取代反应实验装置图,具体的实验方法是:
取一个100 mL的大量筒,先后收集20 mL CH4和80 mL Cl2,进行实验。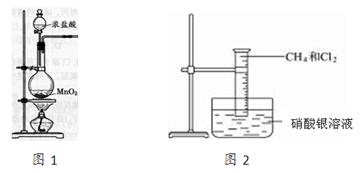
(1)实验室制取氯气的装置如上图1所示,请写出烧瓶中的反应方程式为:
。浓盐酸在反应中体现了
性和性。
(2)下列常用的干燥剂中,不能干燥氯气的是。
| A.浓硫酸 | B.P2O5 | C.无水氯化钙 | D.碱石灰 |
(3)氯气是色的有毒气体,实验中剩余的氯气可用NaOH溶液吸收,请写出发生的离子方程式:。
(4)若研究甲烷与氯气的取代反应,还需要的条件是___________。若将如图2所示装置放在强光下照射会有_________________(填可能发生的不良后果)。
(5)若量筒中的甲烷和氯气的量比较大,放在光亮的地方足够长的时间,下方水槽中的现象是_________________________________,产生此现象的原因是:__________________________(用简要的文字和方程式说明)。
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。请填写下列空白:
[实验一]用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。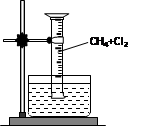
(1)该反应的化学方程式为;(只写第二步)
(2)水槽中盛放的液体最好为;(填标号)
| A.水 | B.饱和石灰水 | C.饱和食盐水 | D.饱和NaHCO3溶液 |
[实验二]用排蒸馏水法收集一试管甲烷和氯气的混合气体,光照反应后,
滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成。
(3)该实验设计的错误之处;
[实验三]
步骤一:收集半试管氯气,加入10 mL 蒸馏水,充分振荡,采用DIS系统的pH传感器测溶液的pH(下同)。测得pH = 3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,加入10 mL 蒸馏水,充分振荡,测得pH = 1.00。
(4)判断该反应中有氯化氢生成的依据是;
(5)假设氯气完全参与反应,且不考虑氯气溶解于水。往反应后的溶液中加水稀释到100.00 mL,取20.00 mL稀释液,加入10.00 mL浓度为0.01 mol·L-1的AgNO3溶液恰好完全反应,则试管中原有氯气在标准状况下的体积为mL;