应用元素周期律的有关知识,可以预测我们不知道的一些元素及其化合物的性质。下列预测中不正确的是( )
①Be的最高价氧化物的水化物可能具有两性
②H2Se是无色,有毒,比H2S稳定的气体
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤SrSO4是难溶于水的白色固体
⑥B和Si的最高价氧化物的水化物均为H2XO3形式,且酸性很弱
| A.①②③④ | B.②④⑥ | C.①③⑤ | D.②④⑤ |
恒温、恒容的条件下对于N2(g)+3H2(g) 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为( )
| A.断开一个N≡N键的同时有6个N—H键生成 |
| B.混合气体的密度不变 |
| C.混合气体的压强不变 |
| D.N2、H2、NH3分子数之比为1:3 :2的状态 |
按下图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )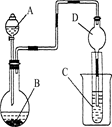
| A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色。 |
| B.若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液变浑浊。 |
| C.实验仪器D主要起到洗气的作用。 |
| D.若A为浓氨水,B为生石灰,C中AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解。 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如右图所示。下列说法正确的是( )
| A.元素X与元素Z的最高正化合价之和的数值等于8 |
| B.元素Y、W的气态氢化物的稳定性,前者比后者差 |
| C.离子Y2-和Z3+的离子半径,后者比前者大 |
| D.元素W的最高价氧化物对应的水化物酸性比Q的强 |
已知温度T时水的离子积常数为KW。该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是()
| A.a = b |
| B.混合溶液的pH = 7 |
C.混合溶液中,c(H+) = 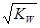 mol/L mol/L |
| D.混合溶液中,c(H+) + c(B-) = c(OH-) + c(A-) |
下列说法中正确的是()
| A.医用酒精的浓度通常为95% |
| B.单质硅是将太阳能转变为电能的常用材料 |
| C.淀粉、纤维素和油脂都属于天然高分子化合物 |
| D.合成纤维和光导纤维都是新型无机非金属材料 |