侯氏制碱法为纯碱工业的发展做出了杰出的贡献.用此方法制得的工业纯碱产品中会含有一定量的氯化钠.为测定一种用侯氏制碱法生产的工业纯碱产品中碳酸钠的纯度,现取
该工业纯碱样品.加入
某溶质质量分数的稀盐酸,恰好完全反应,得到
不饱和溶液.请回答下列问题:
(1)加入稀盐酸发生反应的化学方程式为
(2)求解样品中碳酸钠质量
的比例式为
(3)样品中碳酸钠的纯度为
(4)若向反应后的溶液中加入
水,则所得溶液中溶质和溶剂的质量最简比为
(5)工业上常用碳酸钠和氢氧化钙反应来制取氢氧化钠,若要用这种方法制得
含氢氧化钠
的工业烧碱,需要上述用侯氏制碱法获得的工业纯碱产品的质量是
某造纸厂排放的废水中含有Na2CO3和NaOH。为了测定废水中Na2CO3的质量分数,取废水150g,逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如下图所示(提示:NaOH+HCl=NaCl+H2O,Na2CO3 + 2HCl =" 2NaCl" + H2O + CO2↑) 。该废水中Na2CO3的质量分数和所用稀盐酸中溶质的质量分数分别是多少?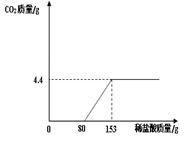
(3分)在科学家眼里,二氧化碳是可以利用的重要资源。在一定条件下,二氧化碳和金属钠反应可以制金刚石,反应的化学方程式为CO2+4Na C(金刚石)+2Na2O。请计算46 g金属钠理论上可制得金刚石的质量。
C(金刚石)+2Na2O。请计算46 g金属钠理论上可制得金刚石的质量。
氯酸钾和二氧化锰共热制取氧气,已知反应前混合物共15.5g,反应完全后剩余固体10.7g,问分解出氧气多少克?剩余固体混合物中二氧化锰多少克?(友情提示:化学方程式为2KClO3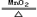 2 KCl + 3O2↑)
2 KCl + 3O2↑)
中国登山协会为纪念我们首次攀登珠穆朗玛峰成功50周年,再次组织攀登珠峰活动。阿旺扎西等一行登山运动员于2003年5月21日13:40成功登顶。假如每位运动员冲顶时消耗自带的液氧4.8kg。求:若在实验室以高锰酸钾为原料制取相同质量的氧气,需要多少千克的高锰酸钾?
根据氧化铁(Fe2O3)的化学式计算:
(1) 氧化铁的相对分子质量为。
(2) 氧化铁里铁元素跟氧元素的质量比为。
(3)铁元素的质量分数为。