在某温度下,将 和
和 各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定
各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定 的变化,5S时测定
的变化,5S时测定 =0.0080mol/L并保持不变。H2+I2(g)
=0.0080mol/L并保持不变。H2+I2(g)  2HI(g)
2HI(g)
(1)反应的平衡常数的表达式是 = ;
= ;
(2)此温度下,平衡常数值为 ;
(3)若在此温度下,在10L的密闭器充入0.2molHI气体,达到平衡时,HI的转化率为 。
金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点上各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有(见图1-25)。金原子的直径为d,用NA表示阿伏加德罗常数,M表示金的摩尔质量。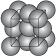
图1-25
(1)金晶体每个晶胞中含有 个金原子。
(2)欲计算一个晶胞的体积,除假定金属原子是刚性小球外,还应假定 。
(3)一个晶胞的体积是 。
(4)金晶体的密度是 。
将2.80 g CaO与500 mL某浓度的盐酸充分反应,将所得溶液平均分成两份。向其中一份中加入足量的AgNO3溶液,生成的沉淀干燥后的质量为14.4 g;向另一份溶液中加入足量Zn粒,产生0.560 L(标准状况)气体。计算所用盐酸中HCl的物质的量浓度。
将某温度下的KNO3溶液200 g蒸发掉10 g水,恢复到原温度,或向其中加入10 g KNO3固体,均可使溶液达到饱和。试计算:
(1)该温度下KNO3的溶解度。
(2)原未饱和溶液中溶质的质量分数。