常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH,如下表:
| 实验编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.2 |
0.1 |
pH<7 |
请回答:
(1)从①组情况分析, HA是强酸还是弱酸 。
(2)②组情况表明,c 0.2 (选填“大于”、“小于”或 “等于”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是 。
(3)从③组实验结果分析,说明HX的电离程度______NaX的水解程度(选填“大于”、“小于”或 “等于”),该混合溶液中离子浓度由大到小的顺序是 。
(4)①组实验所得混合溶液中由水电离出的c(OH-)= mol·L-1。写出该混合溶液中下列算式的精确结果(不能作近似计算)。
c(Na+)-c(A-)= mol·L-1 ;c(OH-)-c(HA)= mol·L-1
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,则氧化剂与氧化产物的物质的量之比为。
(2)上述反应中产生的气体可用吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3— = 2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成48g S,则生成标准状况下的NO2的体积为L。若准确测得的实际体积小于理论值(计算值),请分析可能原因。
(4)某课外活动小组设计了以下实验方案验证Ag与浓HNO3反应的过程中可能产生NO。其实验流程图如下: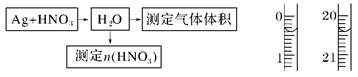
①测定硝酸的物质的量:
反应结束后,从如图B装置中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如上图所示。在B容器中生成硝酸的物质的量为。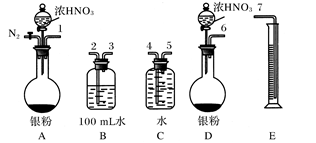
②测定NO的体积:
若实验测得NO的体积为112.0 mL(已折算到标准状况),则Ag与浓硝酸反应的过程中(填“有”或“没有”)NO产生,作此判断的依据是。
已知A、B、E是常见的非金属单质,C是导致酸雨的主要成分之一,Y是生活中常见的金属单质。D、K是重要的无机化工产品。X含有两种元素,具有摇篮式的分子结构,其球棍模型如图所示。H为白色沉淀。下列转化关系中部分反应条件和产物略去。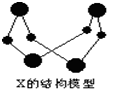
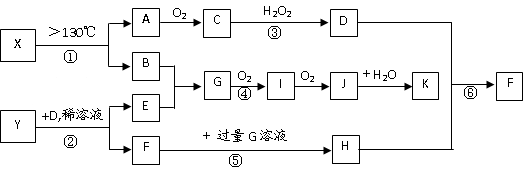
试回答下列问题
(1)X的化学式为: ▲ ;G的电子式 ▲ ;
(2)反应④的化学方程式:▲;
反应③的离子方程式: ▲;
(3)①~⑥反应中属于氧化还原反应的是(填编号) ▲;
(4)已知在真空中,将A与CuO按物质的量1:1反应可生成A2O。写出该反应的化学方程式:▲;
(5)依据实验中的特征实验现象,可确定Y是何种金属,该实验现象为▲。
(16分)能源危机是当前全球问题,开源节流是应对能源危机的重要举措。
⑴下列做法有助于能源“开源节流”的是▲(填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如右图所示。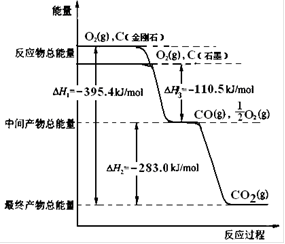
(a)在通常状况下,金刚石和石墨中____▲___(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为____▲___ kJ·mol-1。
(b)12 g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量 ▲kJ。
(3)已知:N2(g)+O2(g)=2NO(g);ΔH=+180.0 kJ·mol-1。
综合上述有关信息,请写出CO除NO的热化学方程式▲ 。
美国斯坦福大学研究人员最近发明一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电。
(4)研究表明,电池的正极用二氧化锰纳米棒为材料可提高发电效率,这是利用纳米材料具有
▲ 特性,能与钠离子充分接触。
(5)海水中的“水”电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池负极反应式为▲;当生成1 mol Na2Mn5O10转移▲ mol电子。
溴被称为“海洋元素”。已知Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。实验室模拟从海水中提取溴的主要步骤为:
步骤1:将海水蒸发浓缩除去粗盐;
步骤2:将除去粗盐后的母液酸化后,通入适量的氯气,使Br-转化为Br2;
步骤3:向步骤2所得的水溶液中通入热空气或水蒸气,将溴单质吹入盛有二氧化硫水溶液的容器中;
步骤4:再向该容器中通入适量的氯气,使Br-转化为Br2;
步骤5:用四氯化碳萃取溴单质,经分液、蒸馏得粗溴。
(1)步骤3中的反应的离子方程式▲。
(2)步骤2中已经制得了溴,还要进行步骤3和步骤4的原因是▲。
(3)步骤5中萃取和分液所需要的主要玻璃仪器为▲。 (4)用如上图所示的实验装置可精制粗溴。
(4)用如上图所示的实验装置可精制粗溴。

 ①反应过程中需要对A容器加热,加热的方法是▲。
①反应过程中需要对A容器加热,加热的方法是▲。
图中冷却水应从B的▲口进入(填“a”或“b”)。
②C中加冰的目的是▲。
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)
(1) 若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为,
反应④的化学方程式为:。
(2) 若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是,
在常温下,1g D与F反应生成B时放出92.3kJ热量,写出该反应的热化学方程式。
(3) 若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为,分子E的结构式为。