X、Y、Z、M、G五种元素分属三个短周期, 且原子序数依次增大。X、Z同主族, 可形成离子化合物ZX; Y、M同主族, 可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式), 非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有 、 (写出其中两种物质的化学式,一种为单质,另一种为化合物)。
(4)ZX的电子式为 。
(5)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下图),反应原理为:
2Z+ FeG2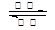 Fe+ 2ZG
Fe+ 2ZG
放电时, 电池的正极反应式为 ,充电时, (写物质名称)电极接电源的负极。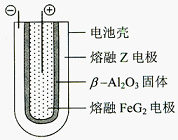
现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示。请回答下列问题: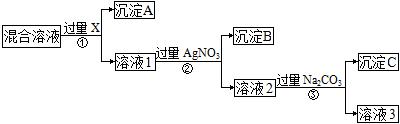
(1)试剂X最好是 (填化学式),检验X是否加入过量的方法 。
(2)写出步骤②的离子反应方程式 。
(3)按此实验方案得到的溶液3中肯定含有________(填化学式)杂质;为了除这个杂质,可以向溶液3中加入过量的________,之后若要获得纯固体NaNO3,还需进行的实验操作是___________(填操作名称)。
下图所示是分离混合物时常用的仪器,回答下列问题: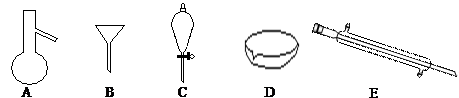
(1)写出上述仪器的名称A ,C ,E 。
(2)分离以下混合物应该主要选用上述什么仪器?(填字母符号)
①粗盐和泥沙: ;②花生油和水: 。
(3)关于仪器的使用,下列说法不正确的是 。
| A.A仪器可以用酒精灯直接加热 |
| B.B仪器可以用于过滤 |
| C.C仪器在放出液体时应打开上边的塞子 |
| D.在实验室应用D仪器进行实验时要不断用玻璃棒搅拌 |
E.蒸馏时,E仪器中水的流向是上口进,下口出
(4)若向C装置中加入碘水和足量CCl4,充分振荡后静置,会观察到什么现象? 。
(1)常温下,将pH=10和pH=12的NaOH溶液以1∶1的体积比混合,则混合后所得溶液的pH约为________。
(2)0.2 mol·L-1 NaHSO4和0.1 mol·L-1 BaCl2溶液按等体积混合后,则溶液的pH等于________。
(3)用pH=4和pH=11的强酸和强碱混合,使pH=10,则两溶液的体积比为________。
泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈碱性的原因是:_____________;灭火器内另有一容器中装有Al2(SO4) 3溶液,该溶液呈酸性的原因是:____________。当意外失火时,使泡沫灭火器倒过来即可使药液混合,喷出CO2和Al(OH)3,阻止火势蔓延。其相关的化学方程式为:_________________。
25 ℃时,合成氨反应的热化学方程式为:
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4 kJ/mol
(1)在该温度时,取l mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4 kJ。其原因是 。
(2)为了提高NH3的产率,应如何选择反应条件?