已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平②2CH3CHO+O2 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
回答下列问题:
(1)写出A的电子式 。
(2)B、D分子中的官能团名称分别是 、 。
(3)写出下列反应的化学方程式及反应类型:
① ,属于________________反应;
② ,属于________________反应;
④ ,属于________________反应。
(1)①液态HCl②BaSO4③氯水④无水乙酸⑤SO2⑥熔融的KCl⑦Cu⑧酒精溶液上述物质属于电解质的是能导电的是
属于强电解质的是属于非电解质的是
(2)在标准状况下a. 6.72L CH4气体 b.3.01×10 23个HCl气体分子 c.13.6g H2S气体 d.0.2molNH3,下列对这四种气体的关系从大到小的排列是(用上述序号表示)
23个HCl气体分子 c.13.6g H2S气体 d.0.2molNH3,下列对这四种气体的关系从大到小的排列是(用上述序号表示)
①四种气体的物质的量,
②标准状况下四种气体的体积,
③四种气体的质量。
(3)化合物A是一种不稳定的物质,它的分子组成可用 表示。10mLA气体能分解生成15mL
表示。10mLA气体能分解生成15mL 和10mL
和10mL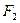 (同温、同压)。
(同温、同压)。
A的化学式是___________。推断理由是___________。
某工厂实验室用CO和H2制备CH3OH,其原理为:
CO(g)+2H2(g)  CH3OH(g)△H < 0
CH3OH(g)△H < 0
试回答下列问题:
(1)若该反应在298K、398K时,化学平衡常数分别为K1、K2,则K1 K2(填“>”、“<”、“=”)
(2)在恒温恒容条件下,判断该反应达到化学平衡状态的是
| A.v正(H2)=2 v正(CH3OH) | B.v正(H2)=v正(CO) |
| C.容器内压强保持不变 | D.混合气体的密度不变 |
(3)某温度下,向一定容积的密闭容器中充入CO和H2,浓度分别为1mol/L和2mol/L,达到平衡时CO的 浓度为0.6mol/L,试求该温度下的化学平衡常数。
浓度为0.6mol/L,试求该温度下的化学平衡常数。
向Na2CO3溶液中滴加酚酞呈红色的原因是 (用离子方程式表示);溶液中各离子浓度由大到小的顺序;向此溶液中加入AlCl3溶液,观察到的现象是,反应的离子方程式为。
(用离子方程式表示);溶液中各离子浓度由大到小的顺序;向此溶液中加入AlCl3溶液,观察到的现象是,反应的离子方程式为。
(10分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) 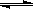 CH3OH(g)
CH3OH(g)
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=,升高温度,K值(填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a. 氢气的浓度减少 b. 正反应速率加快,逆反应速率也加快
c. 甲醇的物质的量增加 d. 重新平衡时n(H2)/n(CH3OH)增大
(4)据研 究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:(用化学方程式表示)
究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:(用化学方程式表示)
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
C(s)+H2O(g)  CO(g)+H2(g)ΔH=+131.3 kJ•mol-1,ΔS=+133.7J•(K•mol) -1
CO(g)+H2(g)ΔH=+131.3 kJ•mol-1,ΔS=+133.7J•(K•mol) -1
①该反应能否自发进行与有关;
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是(填字母,下同)。
a.容器中的压强不变 b.1 mol H —H键断裂的同时断裂2 molH—O键
—H键断裂的同时断裂2 molH—O键
c.v正(CO) = v逆(H2O) d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应 CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所 需时间/min |
||
| H2O |
CO |
H2 |
CO |
|||
| 1 |
650 |
2 |
4 |
1.6 |
2.4 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
1.6 |
3 |
| 3 |
900 |
a |
b |
c |
d |
t |
①实验1中以v(CO2) 表示的反应速率为 。
。
②该反应的逆反应为 (填“吸”或“放”)热反应
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:
CO2(g)+3H2(g)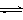 CH3OH(g)+H2O(g) ,右下图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c (CH3OH)增大的是___________。
CH3OH(g)+H2O(g) ,右下图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c (CH3OH)增大的是___________。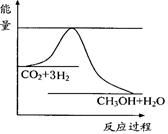
a.升高温度
b.充入He(g ),使体系压强增大
),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1mol CO2和3mol H2