关于下列各实验装置的叙述中,不正确的是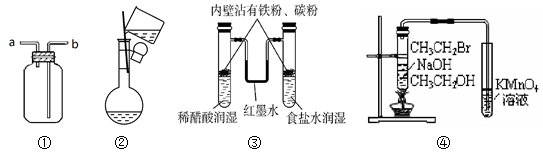
| A.装置①:a口进气可收集CO2,b口进气可收集NH3 |
| B.装置②:配制一定物质的量浓度溶液时,转移溶液 |
| C.装置③:模拟铁锈蚀 |
| D.装置④:证明CH3CH2OH发生消去反应生成了乙烯 |
为了除去蛋白质溶液中混有的少量食盐,应采取的方法是
| A.渗析 | B.过滤 | C.电泳 | D.丁达尔效应 |
下列关于测定胆矾晶体里结晶水含量的实验操作,会引起测定结果偏高的是
| A.加热时,强热蒸干,硫酸铜表面出现黑色固体 |
| B.坩埚内附着有少量氯化钠固体 |
| C.加热时,胆矾晶体未完全变白即停止加热 |
| D.加热胆矾晶体后在空气中冷却称量 |
环境监测测定水中溶解氧的方法是①量取a mL水样迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH)塞好盖子,摇匀,使之完全反应;②测定:开塞后加适量H2SO4,使之生成I2,再用6 mol/L的Na2S2O3溶液和I2恰好完全反应,消耗3 V mL Na2S2O3溶液,有关方程式为:2Mn2++ O2 + 4OH-= 2MnO(OH)2(快)
MnO(OH)2 + 2I-+ 4H+= Mn2++ I2 +3H2O
I2 + 2Na2S2O3 =" 2NaI" + Na2S4O6
求:水中溶解氧的量(g/L为单位)()
A. |
B.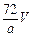 |
C.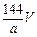 |
D.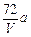 |
在容积为672 mL的烧瓶中充满NO、NO2的混合气体,将其倒立在水槽里,去塞后通入280 mL氧气,反应恰好完成,且水充满烧瓶(气体体积都已合折为标准状况),下列有关叙述中正确的是()
| A.总反应:NO + NO2 + O2 + H2O = 2HNO3 |
| B.总反应:4NO + 8NO2 + 5O2 + 6H2O = 12HNO3 |
| C.生成HNO3浓度接近0.03 mol/L |
| D.生成HNO3浓度约0.45 mol/L |
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是()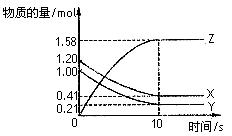
| A.反应开始到10s,Z表示的反应速率为0.158moL/(L·s) |
| B.反应开始到l0s时,平均反应速率: v(X) = v(Y) = 0.0395 mol/(L·s) |
C.反应的化学方程式为:2Z(g) X(g)+Y(g) X(g)+Y(g) |
| D.l0 s后,该反应停止进行 |