(共6分)如图所示,有三种固体物质的溶解度曲线,请你完成下列填空: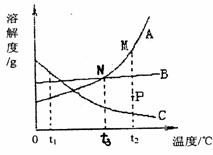
(1)图中N点表示的意义是 。
(2)t2℃时,A、B、C 三种物质的溶解度大小关系为 。
(3)把 t3℃时等质量的三种物质的饱和溶液升高温度至t2℃,则此时三种溶液的溶质质量分数大小关系是 。
化学实验培养了我们科学的思维方法,也增强了我们学习化学的兴趣.为了便于研究,我们可以把化学实验从“实验装置、物质的性质、探究的方法”等角度进行分类.现有如下实验: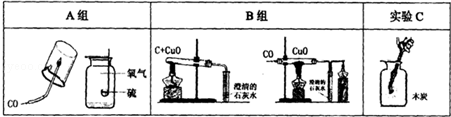
若请你将实验C归类,你会选择组(填“A”或“B”),理由是.
用 分别表示氢原子和氧原子,下图表示过氧化氢溶液分解的微观模拟图,结合图示回答问题:
分别表示氢原子和氧原子,下图表示过氧化氢溶液分解的微观模拟图,结合图示回答问题: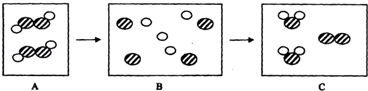
C属于物质分类的(填“混合物”或“纯净物”),请从微观角度说出你的判断依据从微观角度解释由B到C变化的实质.
目前,在所有节能与新能源车型中,混合动力车型相对成熟.当前的混合动力汽车一般是指内燃机车发电机,再加上蓄电池的汽车.根据上述信息,回答问题:该汽车外壳由钢制成,主要是利用钢具有的物理性质;推广使用混合动力汽车的目的是;此种汽车行驶过程中主要是利用小型的内燃机燃烧汽油(主要成分为辛烷:C8H18)来提供动力,请你写出辛烷燃烧的化学方程式;反应前后氧元素的化合价分别为当爬坡或遇路况不好时,蓄电池开始工作来补充动力,蓄电池工作时的能量转化为.
合理饮食,荤素搭配”是我们健康的生活理念,请用学过的化学知识回答问题;
我们每餐都吃米饭(或馒头)等主食,主要是为人体补充营养素;该营养素的作用是;为了使蔬菜叶色浓绿,应施加的化肥种类是肥,刚用熟石灰改良过的酸性土壤施加此类化肥时应注意.
归纳、分类是学习化学的重要方法.请根据化学式的意义从H2、P2O5、02、NO2、Fe、O3六种物质中选出部分物质归为一类,回答下列问题:
(1)选出的一组物质的化学式有
(2)分类的依据是.