非金属单质A经下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题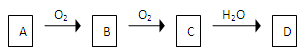
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体
①D的化学式是 。
②在工业生产中,大量排放的B气体被雨水吸收后形成 而污染环境
(2)若A在常温下为气体,C是红棕色气体。
①A、C的化学式分别是 ; 。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式
。
该反应 (填属于或不属于)氧化还原反应。
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)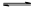 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压强(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体总浓度(×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判断该分解反应已经达到化学平衡的是___________。
A.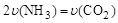 B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:_______________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量______(填“增加”、“减小”或“不变”)。
(2)已知:NH2COONH4+2H2O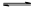 NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。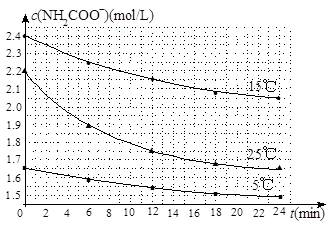
④计算25℃时,0~6min氨基甲酸铵水解反应的平均速率_____________________。
⑤根据图中信息,如何说明水解反应速率随温度升高而增大:_________________。
我国《车用燃料甲醇国家标准》的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过将煤的气化过程中生成的CO和H2在一定条件下发生如下反应制得:CO(g) + 2H2(g) 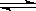 CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。
CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。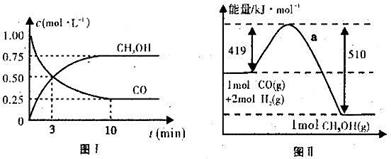
请根据图示回答下列问题:
(1)图I是反应时CO和CH3OH的浓度随时间的变化情况,从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=_______________。
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线a表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b。
(3)写出该反应的热化学方程式。
(4)该反应的平衡常数K的表达式为;当温度升高时,该平衡常数K将________(填“增大”、“减小”或“不变”)。
(5)恒容条件下,下列措施中能使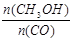 增大的有。
增大的有。
A.升高温度 B.充人He气
C.再充入1molCO和2molH2 D.使用催化剂
(6)在恒温条件下,保持CO浓度不变,扩大容器体积,则平衡(填“逆向移动”、“正向移动”、“不移动”)
(7)在温度、容积相同的三个密闭容器中,按不同方式投料,保持恒温、恒容,测得反应达到平衡时的有关数据如下
| 容器 |
甲 |
乙 |
丙 |
| 投料量 |
1mol CO 、2mol H2 |
1molCH3OH |
2molCH3OH |
| CH3OH的浓度(mol·L-1) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
放出Q1kJ |
吸收Q2kJ |
吸收Q3kJ |
| 体系压强(Pa) |
P1 |
P2 |
P3 |
| 反应物转化率 |
α1 |
α2 |
α3 |
则下列关系正确的是
A.c1= c2 B.Q3= 2Q2 C.2 P1<P3
D.α1+α2=1 E.2α2=α3
E.2α2=α3
F.该反应若生成1molCH3OH放出的热量为(Q1+ Q2)kJ
(8)若在一体积可变的密闭容器中充入1mol CO、2mol H2和1molCH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向(填“正”、“逆”)反应方向移动,理由是
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)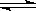 CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表,回答下列问题:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表,回答下列问题:
| T℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(1)该反应正向为ΔH0;若该反应符合如图所示的关系,则在图中,Y轴是指。(答出一种即可)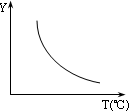
(2)能判断该反应达到化学平衡状态的依据是(多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v (H2)正=v (H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: 0.9·c(CO2)·c(H2)=c(CO)·c(H2O),由此可以判断此时的温度为℃。其它条件不变,升高温度,原化学平衡向反应方向移动(填“正”或“逆”),容器内混合气体的平均相对分子质量(填“增大”、“减小”或“不变”)。
(7分)请回答下列有关金属的问题。
(1)铝是活泼金属,通常铝锅却很耐腐蚀,原因是。
(2)右边是某探究实验装置图。一段时间后,能观察到现象(装置气密性良好,且开始时U型管两端的红墨水液面相平)。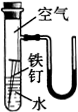
(3)X、Y、Z是三种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化。
①X、Y、Z和银四种金属的活动性由强到弱的顺序是。
②具体确定一种X后,写出X与硝酸银溶液反应的化学方程式。
右图是某包装袋上的部分文字说明。
(1)这里的钙、铁、磷、锌指的是(填“分子”、“原子”或“元素”等)。
(2)这袋奶粉中含蛋白质的质量为_______g。