某元素的原子结构示意图为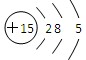 ,则该元素的位置为( )
,则该元素的位置为( )
| A.第3周期,第ⅤA族 | B.第2周期,第ⅤA族 |
| C.第3周期,第ⅣA族 | D.第2周期,第ⅠA族 |
可以用来判定碳酸氢钠粉末中混有碳酸钠的实验方法是
| A.加热时有无色气体放出 |
| B.滴加盐酸时有气泡放出 |
| C.溶于水后,滴加稀的氯化镁溶液有白色沉淀生成 |
| D.溶于水后,滴加澄清石灰水有白色沉淀生成 |
下列关于钠的氧化物的叙述正确的是
| A.Na2O2是白色固体,和冷水作用得到O2和NaOH |
| B.Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水 |
| C.Na2O不稳定,能继续被O2氧化生成Na2O2 |
| D.都能与酸反应,生成含氧酸盐,都是碱性氧化物 |
下列有关钠的叙述正确的是
①钠在空气中燃烧生成氧化钠②金属钠可以 保存在煤油中
保存在煤油中
③钠与硫酸铜溶液反应,可以置换出铜④金属钠有强还原性
⑤钠原子的最外层上只有一个电子,所以在化合物中钠的化合价显+1价
| A.①②④ | B.②③⑤ |
C.①④⑤ | D.②④⑤ |
下图是 10ml 量筒的一部分,数字XY之间相差 1ml,若 X=5,则量筒所盛液体的体积是
| A.5.7 ml | B.4.4 ml | C.4.3 ml | D.6.3 ml |
量取100mL碘的饱和水溶液,倒入分液漏斗中,然后再注入4mL四氯化碳,用力振荡后静置,实验现象为
| A.液体分层,上层为四氯化碳层,黄色 |
| B.液体分层,上层为水层,紫色 |
| C.液体分层,下层为四氯化碳层,紫色 |
| D.液体分层,下层为水层,黄色 |