镍(Ni)可形成多种配合物,且各种配合物均有广泛的用途。
(1)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于________晶体;写出两种与配体CO互为等电子体的粒子的化学式________、________。
(2)某镍配合物结构如下图所示,分子内含有的作用力有________(填序号)。
| A.氢键 | B.离子键 | C.共价键 | D.金属键 E.配位键 |
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应,如
① ②
② 、③
、③ 、④ HCHO等,其中碳原子采取sp2杂化的分子有________(填序号);HCHO分子的空间构型为________ 。
、④ HCHO等,其中碳原子采取sp2杂化的分子有________(填序号);HCHO分子的空间构型为________ 。
(4)据报道,含有镁、镍和碳三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为________。晶体中每个镁原子周围距离最近的镍原子有________个。
“比较法”是化学研究的基本方法之一,请运用比较法解答下列问题:已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如: 2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO=Na2CO3。
(1)试分别写出Na2O2与SO2、Na2O2与SO3(g)反应的化学方程式:
、
(2)当1 mol SO3(g)参加反应时,转移电子的物质的量为mol。
(3)通过比较可知:在氧化物中,当非金属元素处于(填“最低”、“中间”或“最高”)价时,其氧化物与过氧化钠反应就有O2生成。
A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是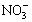 、S
、S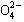 、Cl—、C
、Cl—、C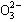 的某一种。
的某一种。
(1)若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
(2)若向(1)的四支试管中分别加盐酸,B盐溶液有沉淀产生,D盐溶液有无色无味气体逸出。
根据(1) 、(2)实验事实可推断它们的化学式为:
A.B.C.D.
(1)下面是唐朝刘禹锡描写沙里淘金的一首诗,其中有的诗句可能包含了化学实验现象或化学实验过程,请在这样的诗句后面写出相应的实验现象或实验过程。
日照澄洲江雾开,
淘金女伴满江隈。
美人首饰王侯印,
尽是沙中浪底来。
(2)某小苏打溶液中含NaHCO3有16.8 g,加入一定物质的量的单质或化合物X,恰好使溶液中溶质只有Na2CO3,且无沉淀产生。请你填写出X的化学式和物质的量。
例如: X为NaOH时,物质的量为0.2 mol ;
①X为时,物质的量为;
②X为时,物质的量为;
有机物A的结构简式是 ,它可以通过不同的反应得到下列物质:
,它可以通过不同的反应得到下列物质:
B. C.
C.
D. E.
E.
(1)E中含氧官能团的名称为。
(2)写出A制取C、D两种物质的有机类型:C、D。
(3)写出由A制取B的化学方程式: 。
。
H是一种香料,可用下图的设计方案合成。
已知:① 在一定条件下,有机物有下列转化关系:
 ② 在不同的条件下,烃A和等物质的量HCl在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
② 在不同的条件下,烃A和等物质的量HCl在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
(1)D的结构简式为。
(2)烃A→B的化学反应方程式是。
(3)E+G→H的化学反应方程式。
(4)H有多种同分异构体,其中含有一个羧基,且其一氯代物有两种的是:
。(用结构简式表示)