氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛的应用。请回答下列问题:
(1)氨气可由N2和H2反应制取,N2(g)+3H2 (g)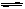 2NH3(g)反应过程的能量变化如图所示:
2NH3(g)反应过程的能量变化如图所示:
已知:1molN2分子中的化学键断裂时需要吸收942kJ的能量;1molH2分子中的化学键断裂时需要吸收436kJ的能量;形成1mol N—H键时释放390.8kJ的能量。
①图中A、C分别表示 、 ,E的大小对该反应 的反应热有无影响? 。
该反应需要用铁触媒作催化剂,加铁触媒会使图中B点升高还是降低? 理由 。
②图中△H= kJ·mol-1。
③如果反应速率ν(H2)为0.15mol· L-1·min-1,则ν(N2)= mol· L-1·min-1 ν(NH3)=
mol·L-1 ·min-1。
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=N2O4(l) △H= -19.5kJ·mol-1
N2H4(l)+O2(g)= N2(g)+2H2O(g)△H= -534.2kJ·mol-1
请写出肼和 N2O4反应的热化学反应方程式 。
(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=______________mol/(L·min)
CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=______________mol/(L·min)

(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右上表。请回答:
①表中3min~4min之间反应处于____________状态;C1数值__________0.08mol/L(填大于、小于或等于)。
②反应在4min~5min问,平衡向逆方向移动,可能的原因是____________(单选),表中5min—6min之间数值发生变化,可能的原因是____________(单选)。
a、增加了水蒸气的量 b、降低温度 c、使用催化剂 d、增加氢气浓度
如图为相互串联的甲乙两个电解池,甲池若为电解精炼铜的装置,请回答:
(1)A极材料和B极材料分别是
a.石墨、精铜 b.石墨、粗铜 c.粗铜、精铜 d.精铜、粗铜
(2)电解质溶液为 。
(3)若甲槽阴极增重12.8g,则乙槽阴极放出气体在标准状况下的体积为 。
(4)若乙槽剩余液体为400mL,求电解后得到碱液的物质的量浓度 。
二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物。综合治理基污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)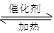 2SO3(g)△H=-198kJ•mol-1
2SO3(g)△H=-198kJ•mol-1
某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示.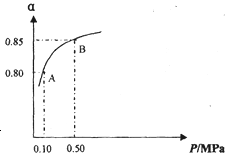
根据图示回答下列问题:
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa.该反应的平衡常数等于 _________________。
②平衡状态由A变到B时.平衡常数K(A)____________K(B)(填“>”、“<”或“=”)
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
若用标准状况下4.48L CH4还原NO2至N2,放出的热量为:____________kJ
(1)常温下某溶液中由水电离出的离子浓度符合c(H+)·c(OH-)=1×10-20的溶液,其pH为____________,此时水的电离受到______________。
(2)已知:2NO2(g)===N2O4(g)ΔH=-57.20 kJ·mol-1。一定温度下,在密闭容器中反应2NO2(g)===N2O4(g)达到平衡。其他条件不变时,下列措施能提高NO2转化率的是__________(填字母)。
A.减小NO2的浓度B.降低温度
C.增加NO2的浓度D.升高温度
(3)在某温度下,H2O的离子积常数为1×10-13 mol2·L-2,则该温度下:
①0.01 mol·L-1NaOH溶液的pH=_____________;
②100 mL 0.1 mol·L-1H2SO4溶液与100 mL 0.4 mol·L-1的KOH溶液混合后,pH=___________。
(4)已知一溶液有4种离子:X+、Y-、H+、OH-,下列分析结果肯定错误的是______________。
A.c(Y-)>c(X+)>c(H+)>c(OH-)B.c(X+)>c(Y-)>c(OH-)>c(H+)
C.c(H+)>c(Y-)>c(X+)>c(OH-) D.c(OH-)>c(X+)>c(H+)>c(Y-)
(5)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl-)。则溶液显___________(填“酸”“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=________________。
(6)水溶液中的行为是中学化学的重要内容。已知下列物质的电离常数值(25 ℃):
HClO:Ka=3×10-8 HCN:Ka=4.9×10-10 H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11
84消毒液中通入少量的CO2,该反应的化学方程式为_____________________。
反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题。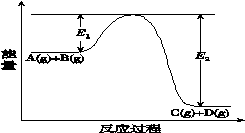
①图中E1代表的意义是_____________________。
该反应是______________反应(填“吸热”或“放热”)。反应热ΔH的表达式为________________。
②当反应达到平衡时,升高温度,A的转化率______________(填“增大”“减小”或“不变”)。
(2)800 ℃时,在2 L密闭容器内充入0.50 mol NO和0.25 mol O2,发生如下反应:2NO(g)+O2(g)===2NO2(g)ΔH<0。体系中,n(NO)随时间的变化如下表:
| t/s |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)/mol |
0.50 |
0.35 |
0.28 |
0.25 |
0.25 |
0.25 |
①能说明该反应已达到平衡状态的是______________。
A.v(NO2)正=v(O2)逆B.容器内压强保持不变
C.v(NO)逆=2v(O2)正 D.容器内气体颜色不变
②能使该反应的反应速率增大,且平衡向正反应方向移动的措施是______________。
A.适当升高温度 B.缩小反应容器的体积
C.增大O2的浓度D.选择高效催化剂