导电薄膜属高分子材料,其结构片断为…CH=CH―CH=CH―CH=CH―CH=CH…由此判断合成导电薄膜的单体为( )
| A.乙炔 | B.乙烷 | C.乙烯 | D.1,3-丁二烯 |
化合物C是制备液晶材料的中间体之一,它可由A和B在一定条件下制得
下列说法正确的是
| A.可用FeCl3溶液检验C中是否含有B |
| B.1molC分子最多可与4molH2发生加成反应 |
| C.可以用酸性KMnO4溶液检验B中是否含有-CHO |
| D.1molC与NaOH溶液反应时最多消耗1molNaOH |
下述实验能达到预期目的的是
| 编号 |
实验内容 |
实验目的 |
| A |
向甲苯中滴入少量浓溴水,振荡,静置,溶液分层,下层几乎无色 |
验证甲苯和溴发生取代反应,使溴水褪色 |
| B |
在混有少量苯酚的苯中滴加足量溴水,充分振荡后过滤 |
除去苯中少量的苯酚 |
| C |
溴乙烷与NaOH溶液加热至不再分层,冷却后加稀硝酸至酸性,再滴加AgNO3溶液 |
验证卤素原子为溴 |
| D |
将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 |
检验气体中含有乙烯 |
下列化合物的分子中,所有原子都处于同一平面的有
| A.环己烷 | B.对二甲苯 | C.间二氯苯 | D.四氟乙烯 |
某有机物的结构简式为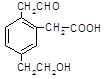 ,它在一定条件下可能发生的反应是
,它在一定条件下可能发生的反应是
①加成;②水解;③酯化;④氧化;⑤中和;⑥消去;⑦还原
| A.①③④⑤⑥⑦ | B.①③④⑤⑦ | C.①③⑤⑥⑦ | D.②③④⑤⑥ |
下列离子方程式正确的是
A.氯乙烷与氢氧化钠醇溶液共热:C2H5Cl+OH- C2H5OH+Cl- C2H5OH+Cl- |
| B.溴乙酸与热氢氧化钠溶液反应:BrCH2COOH+OH-=BrCH2COO-+H2O |
| C.苯酚钠溶液中通入少量CO2:2C6H5O-+H2O+CO2→2C6H5OH+CO32- |
| D.乙醛与氢氧化铜碱性悬浊液共热: |
CH3CHO+2Cu(OH)2+OH- CH3COO—+Cu2O↓+3H2O
CH3COO—+Cu2O↓+3H2O