工业上从海水中提取溴的方法如下:
①将蒸馏(制淡水)后浓缩的海水用硫酸进行酸化;
②向酸化的海水中通入足量氯气,使溴离子转化为溴单质;
③向上述溶液中通入空气和水蒸气,将溴单质吹入盛有二氧化硫水溶液的吸收塔内转化成氢溴酸;④向吸收塔内通入适量的氯气;
⑤用四氯化碳萃取吸收塔中的溴单质。
请完成下列问题:
(1)在实验室中蒸馏海水制淡水时,常用的仪器除了酒精灯、锥形瓶、牛角管、冷凝管、石棉网及必要的夹持仪器,还需要的玻璃仪器有 ;蒸馏时碎瓷片的作用是____________________。
(2)步骤②中反应的离子方程式为
(3)步骤③的目的是使溴单质富集,试写出溴单质与二氧化硫水溶液反应的化学方程式 。反应中_________(写化学式)是氧化剂。1mol氧化剂在反应中得到 mol电子。
(4)下列能代替四氯化碳来萃取溴的试剂是 (填序号)
| A.盐酸 | B.酒精 | C.乙酸 | D.苯 |
在里或下能导电的化合物叫电解质。电解质溶液之所 以能导电,是由于它们在溶液中发生了,产生了。
以能导电,是由于它们在溶液中发生了,产生了。
粗盐提纯实验中,除去泥沙的三个基本操作是:、、。
硒元素具有抗衰老、抑制癌细胞的功能,其化学性质与硫相似。硒的元素符号为Se,相对原子质量为79,对应的某种含氧酸的化学式为H2SeO3。
(1)这种酸应读作;
( 2)若将二氧化硫通入H2SeO3的溶液中,会有Se析出,写出该反应的化学方程式:
2)若将二氧化硫通入H2SeO3的溶液中,会有Se析出,写出该反应的化学方程式: ;
;
(3)又已知2HCl + H2SeO4 ="=" H2SeO3 + Cl2 + H2O,则H2SeO4、H2SeO3、H2SO3的氧化性由强到弱的顺序是。
为什么日常生活中能用热的纯碱溶液来洗涤沾有油脂的器皿:
下图是某市污水处理的工艺流程示意图: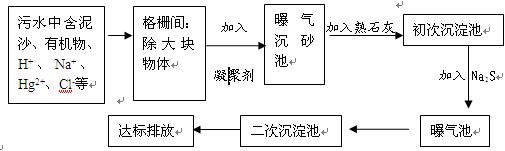
(1)常用的凝聚剂可以是(任填一种凝聚剂的名称)
(2)加入熟石灰的目的是,写出相关的化学方程式。
(3)加入Na2S的作用是。