某化学课外小组用下图装置制取溴苯,先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。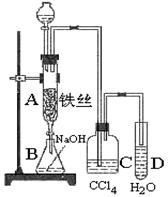
(1)写出A中反应的化学方程式
⑵实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关反应的化学方程式 。
⑶ C中盛放CCl4的作用是 。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明该反应为取代反应。另一种验证的方法是向试管D中加入 ,现象是 。
已知乙醇可以和无水CaCl2反应生成微溶于水的CaCl2•6C2H5OH 。
有关试剂的沸点如下:CH3COOC2H577.1℃; C2H5OC2H534.5℃;
C2H5OH 78.3℃; CH3COOH 118℃。
某课外小组用如下图所示装置制备乙酸乙酯粗产品,试回答下列问题:
(1)蒸馏烧瓶中加入的试剂是:冰乙酸、酒精和浓硫酸,
其中浓H2SO4的作用是和。
(2)冷凝管中最先冷凝的馏分是,弃去低沸点的馏分。收集沸点在76℃~120℃
之间的馏分,将其倾倒入饱和Na2CO3溶液中观察到的现象是:。
上述实验中饱和碳酸钠溶液的作用是_____(填序号)
A.中和乙酸和乙醇;B.中和乙酸并溶解乙醇;
C.加速酯的生成,提高酯的产率 D.有利于分层析出。
(3)写出上述实验中用CH3COOH、CH3CH218OH和浓硫酸制备乙酸乙酯的化学方程式:
。
(4)分离出粗产品乙酸乙酯,再加入无水CaCl2,震荡分离的目的是:
为了干燥乙酸乙酯可选用的最佳干燥剂为 ________(填序号)
A.五氧化二磷 B.无水硫酸钠 C.碱石灰 D.固体氢氧化钠
某化学兴趣小组为探究
的性质,按下图所示装置进行实验。
请到答F列问题:
(1)装置
中盛放亚硫酸钠的仪器名称是,其中发生反应的化学方程式为;
(2)实验过程中,装置
、
中发生的现象分别是,这些现象分别说明
具有的性质是和;装置
中发生反应的离子方程式为;
(3)装置
的目的是探究
与品红作用的可逆性,请写出实验操作及现象;
(4)尾气可采用溶液吸收。
氧化铜有多种用途,如用作玻璃着色剂,油类脱硫剂等,为获得纯净的氧化铜并探究其性质,某同学查找了溶度积数据并通过计算得到有关信息(见下表),用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| 完全沉淀时的pH范围 |
≥9.6 |
≥6.4 |
3~4 |
㈠制备氧化铜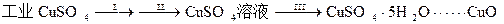
⑴步骤Ⅰ的操作是加入水和少量硫酸溶解样品并过滤,目的是除去不溶性杂质,这一步骤中加酸的作用是。
⑵步骤Ⅱ的操作是:滴加H2O2溶液,稍加热;待反应完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。
①这一步骤的目的是,
②写出加入H2O2溶液时发生反应的离子方程式
③控制溶液pH=3.5的目的是,
⑶步骤Ⅲ的目的是得到CuSO4·5H2O晶体,操作是,水浴加热烘干所得固体。水浴加热的特点是。
㈡探究氧化铜性质
⑴取A、B两支试管,往A中先加入适量CuO粉末,再分别向A和B中加入等体积的3%H2O2溶液,只观察到A中有大量气泡,结论是。
⑵为探究试管A中反应的速率,收集气体并测定其体积必需的实验仪器或装置为。(填写序号)
将绿矾(FeSO4.7H2O)隔绝空气条件下强热分解,已知产物全部为氧化物,为探究绿矾分解的反应产物,某同学进行了以下实验:
实验一:为探究固体产物中Fe元素的价态,该同学将固体产物溶于足量的稀H2SO4得到相应溶液,进行以下猜想和实验
| 猜想 |
实验操作 |
预期现象 |
| 猜想一:Fe元素只显______价 |
①向所得溶液中滴入KSCN溶液 ②向稀酸性KMnO4溶液中滴入所得溶液 |
KSCN溶液无明显现象 |
| 猜想二;Fe元素只显______价 |
稀酸性KMnO4溶液颜色_____ |
|
| 猜想三:Fe元素既有+2价又有+3价 |
KSCN溶液呈______色 稀酸性KMnO4溶液颜色______ |
实验二:为进一步探究该反应的产物,进行了如下图所示的实验
①实验开始时,点燃B处酒精喷灯之前应先打开A处活塞通CO2,其目的是
。
②装置图中C的作用是。
③该组同学称取了55.6克绿矾按如图装置进行试验,待绿矾分解完全后,测得D瓶中沉淀的质量为23.3克,根据这些数据,可以得知,绿矾分解的化学方程式为_____________
④该组同学设计的装置存在着一个明显的缺陷是
单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。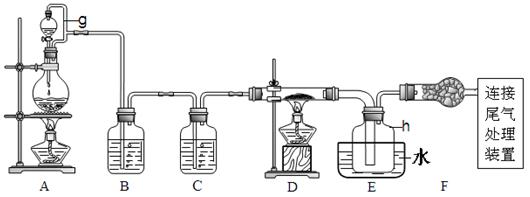
相关信息如下:①四氯化硅遇水极易水解;
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
③有关物质的物理常数见下表:
| 物质 |
SiCl4 |
BCl3 |
AlCl3 |
FeCl3 |
PCl5 |
| 沸点/℃ |
57.7 |
12.8 |
— |
315 |
— |
| 熔点/℃ |
-70.0 |
-107.2 |
— |
— |
— |
| 升华温度/℃ |
— |
— |
180 |
300 |
162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式_____________________________________。
(2)装置A中g管的作用是______________;装置C中的试剂是____________;
装置E中的h瓶需要冷却的理由是__________________________________。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的元素是_____________(填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:
5Fe2++MnO4-+8H+====5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?___(填“是”或“否”),请说明理由_________________
②某同学称取5.000g残留物后,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000×10-2 mol/LKMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的质量分数是_______________。