某校兴趣小组同学进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶装有溶液的试剂瓶未盖瓶盖且标签破损(如下图),于是决定对这瓶溶液进行探究: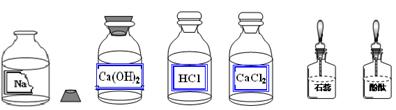
(1)查阅资料:
①酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠;
②氯化钙溶液呈中性
(2)对这瓶溶液到底是氯化钠、氢氧化钠、碳酸钠中的哪一种,同学们根据现有的药品进行如下实验:
①甲同学取待测液于试管中,滴加无色酚酞试液,溶液呈红色,由此得出结论:该溶液不可能是 溶液,理由是 。
②乙同学另取待测液于试管中,滴加稀盐酸,有 的现象,由此得出结论:该溶液是Na2CO3溶液。
③丙同学认为乙同学的结论不严密,因为NaOH溶液露置在空气中,会与 反应生成Na2CO3,反应的化学方程式为 ,所以这瓶溶液还可能是部分变质的NaOH溶液。
④对这瓶溶液的实际成分,小组同学讨论后,一致认为还需要进行如下实验:
设计步骤Ⅰ的目的是:完全除去溶液中的 ,避免其对 的检验造成干扰。
【实验结论】该溶液是 。
(3)拓展运用:
①做实验时,取用药品后应及时 。
②NaOH溶液与盐酸发生中和反应,是 (选填“吸热”或“放热”)反应。
③除去NaOH溶液中混有的少量Na2CO3溶液,可加入适量的 溶液(填序号)。
A.CaCl2 B.HCl C.Ca(OH)2
化学小组同学探究"酸的化学性质",请你参与并完成下列部分实验内容.
| 实验过程 |
实验现象 |
实验结论 |
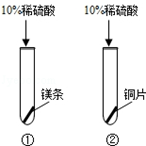 |
①号试管:固体溶解,产生气泡,放热; ②号试管:. |
a、金属活动性: 镁铜(填">"或"<") b、涉及到的化学方程式. |
(2)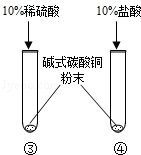 |
③号试管:绿色粉末逐渐溶解,产生气泡,溶液显蓝色. ④号试管:绿色粉末逐渐溶解,产生气泡,溶液显绿色. |
|
【发现问题】碱式碳酸铜与稀硫酸反应形成的
溶液显蓝色,而与盐酸反应形成的
溶液显绿色.
【提出问题】同样都含有
,为什么③号试管中
溶液显蓝色,而④号试管中的
溶液显绿色.
【猜想与假设】猜想一:若溶液中
显蓝色,则
对
显色无影响,而
对
显色有影响;
猜想二:若溶液中
显绿色,则;
猜想三:…
【实验验证】同学们用下列两种不同方案初步验证猜想一,请你补全实验所需试剂:
方案一:取少量③号试管中的溶液于另一支试管中,向其中加入,观察到预期实验现象,猜想一正确.
方案二:取少量④号试管中的
溶液于另一支试管中,向其中加入,观察到预期实验现象,猜想一正确.
【评价与反思】同学们在实验探究的过程中,体会到了溶液颜色成因复杂,相关知识还有待进一步学习.
实验室利用如图所示装置进行相关实验,请回答下列问题: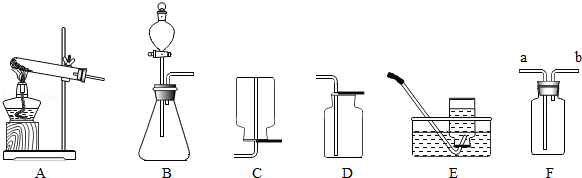
(1)若用高锰酸钾制取氧气,应选用的发生装置是 (填字母);实验结束后,某同学发现水槽中的水变成了浅紫红色,从实验操作角度分析其原因是 ;若用B和D装置制取氧气,B中发生反应的化学方程式: .
(2)若要制取二氧化碳,选用的块状固体药品为 ;若用F装置检验二氧化碳,应在其中装入适量的 ,出现 现象时,证明有二氧化碳产生.
(3)若要制取氢气,可以使用C或E装置收集,能用E装置收集的原因是 ;若选用F装置代替C装置收集氢气,气体应从 (填“a”或“b”)导管口通入.
某兴趣小组同学在实验室将一定量的稀硫酸加入到盛有氢氧化钠溶液的烧杯中,未看到明显的现象.部分同学产生疑问:酸和碱到底能否发生反应?
(1)该小组同学又做了如下实验:
| 实验步骤 |
实验现象 |
实验结论及反应方程式 |
| 向滴有酚酞溶液的稀氢氧化钠溶液的试管中,加入稀硫酸,并振荡 |
观察到溶液由色变为无色. |
氢氧化钠和硫酸发生了反应.反应的化学方程式为 . |
(2)同学们对(1)实验后溶液中的溶质组成展开探究,做出如下猜想:
小明的猜想是:只有
;
小亮的猜想是:有
;
小丽的猜想是:有
;
你认为的猜想不合理.理由是.
若要验证余下两种猜想中的一种是正确的,请完成下面的实验方案.
| 实验步骤 |
预期实验现象 |
实验结论 |
| 取(1)实验后溶液少量于试管中,加入 | 的猜想正确 |
小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(
)与常见金属铁、铜的活动性强弱,邀请你一同参加.
[知识回放]
金属活动性顺序:
,请你在横线上填写对应金属的元素符号.
[作出猜想]
猜想1.
>
>
;猜想2.
>
>
;猜想3.你的猜想是.
[查阅资料]
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(
)溶液.
[设计实验]
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 |
试管1 |
试管2 |
试管3 |
| 实验 操作 |
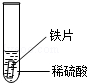 |
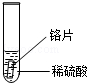 |
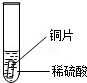 |
| 实验 现象 |
铁片表面产生气泡较慢,溶液变为浅绿色 |
铬片表面产生气泡较快,溶液变成为蓝色 |
[结论与解释]
(1)小聪得到的结论是猜想正确.
(2)实验前用砂纸打磨金属片的目的是.
[知识运用]
将铬片投入
溶液中,反应(填"能"或"不能")进行.若能进行,请你写出反应的化学方程式.
小林同学在做探究质量守恒定律实验时,称取
镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为.实验完毕后,称得所得固体的质量小于
.
【提出问题】固体质量为什么会小于
呢
是否发生了其他反应呢
【查阅资料】镁在空气中燃烧时,除了镁与氧气反应外,还可发生反应:
①
②
【猜想与假设】反应后固体质量小于
是由于发生反应(填"①"或"②")造成的,其理由是.
【实验探究】根据初中化学所学知识用图所示装置除去空气中的氧气得到氮气(含少量稀有气体).可燃物应选择的物质是(填写物质的字母代号).
| A. |
木炭 |
B. |
红磷 |
C. |
硫粉 |
选择的理由是.
将点燃的镁条伸入所制得的氮气中,镁条在氮气中剧烈燃烧.
【实验结论】
镁在空气中完全反应后所得固体质量小于
,是由于生成的产物是的混合物所致.
【评价与反思】通过上述实验,小林对燃烧有了新的认识:.