为了确定SbCl3、SbCl5、SnCl4是否为离子化合物,可以进行下列实验,其中合理、可靠的是( )
| A.观察常温下的状态,SbCl5是苍黄色液体,SnCl4为无色液体。结论:SbCl5和SnCl4都是离子化合物 |
| B.测定SbCl3、SbCl5、SnCl4的熔点依次为73.5℃、2.8℃、-33℃。结论:SbCl3、SbCl5、SnCl4都不是离子化合物 |
| C.将SbCl3、SbCl5、SnCl4溶解于水中,滴入HNO3酸化的AgNO3溶液,产生白色沉淀。结论:SbCl3、SbCl5、SnCl4都是离子化合物 |
| D.测定SbCl3、SbCl5、SnCl4的水溶液的导电性,发现它们都可以导电。结论:SbCl3、SbCl5、SnCl4都是离子化合物 |
A和M为两种元素,已知A位于短周期,且A2-与M+的电子数之差为8,则下列说法正确的是()
| A.A和M原子的电子总数之和可能为11 | B.A和M的原子序数之差为8 |
| C.A和M原子的最外层电子数之和为8 | D.A和M原子的最外层电子数之差为7 |
2001年11月,意大利科学家成功研制出一种新的氧分子(O4),关于O4说法正确的是( )
| A.与O2互为同位素 | B.与O2互为同素异形体 |
| C.是氧元素的新单质 | D.它不是氧的一种单质 |
2002年由德、法、美及波兰等多国科学家组成的科研小组合成了非常罕见的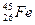 原子,有关
原子,有关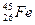 的说法正确的是()
的说法正确的是()
| A.它是一种新元素 | B.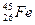 与 与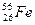 互为同素异形体 互为同素异形体 |
| C.它是一种新核素 | D.这是铁原子发生衰变放出两个质子形成的核素 |
已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,则下列推断不正确的是( )
A.A、B、E一定位于不同周期
B.A、D可能属于同一族
C.D位于第2周期
D.C和D的单质有可能化合形成离子化合物
某元素构成的双原子单质分子有三种,其相对分子质量分别为158、160、162。在天然单质中,此三种单质物质的量之比为1∶1∶1,由此推断以下结论正确的是( )
| A.此元素有三种同位素 | B.其中一种同位素质量数为80 |
| C.其中质量数为79的同位素原子占原子总数的1/2 | D.此元素的各种单质物理性质相同 |