下列各组物质排列不正确的是
| A.酸性强弱: H2SiO3<H2CO3<H2SO4<HClO4 |
| B.离子半径:Na+>Mg2+>Al3+>F- |
| C.碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 |
| D.热稳定性:HF>HCl>H2S>PH3 |
某气态烃在体积恒定的密闭容器中与足量的氧气混合完全燃烧。若反应前后压强保持不变,温度保持在150 ℃,则此烃不可能为
| A.CH4 | B.C2H4 | C.C3H4 | D.C2H6 |
官能团决定有机物的化学特性。下列有机物中,既能使溴水褪色又能跟金属钠反应,还可以和碳酸钠溶液反应的是
绿色化学提倡化工生产应提高原子利用率。原子利用率表示目标产物的质量与生成物总质量之比。在下列制备环氧乙烷(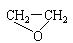 )的反应中,原子利用率最高的是
)的反应中,原子利用率最高的是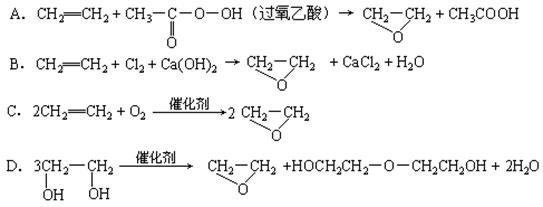
下列反应中生成物总能量低于反应物总能量的是
| A.氢氧化钡晶体和氯化铵晶体混合反应 |
| B.盐酸与金属镁反应 |
| C.石灰石高温煅烧 |
| D.水的分解 |