(1)常温下将0.2 mol/LHCl溶液与0.2 mol/LMOH溶液等体积混合,测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)__________0.2 mol/LHCl溶液中由水电离出的c(H+);(填“>”“<”或“=”)
(2)常温下若将0.2 mol/LMOH溶液与0.1 mol/LHCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度__________MCl的水解程度;(填“>”“<”或“=”)
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH__________。(填“>7”“<7”或“无法确定”)
如图为持续电解含有一定量CaCl2水溶液(含酚酞)的装置(以铂为电极),A为电流表。电解一段时间t1后,将CO2连续通入电解液中。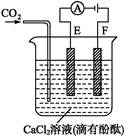
(1)电解时,F极发生 反应,电极反应为 ,E极发生 反应,电极反应为 ,电解总反应为 。
(2)电解池中产生的现象:
① 。
② 。
③ 。
根据如图所示装置回答: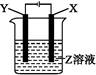
(1)当X为Pt,Y为Fe,Z为AgNO3时,阳极反应为 ,阴极反应为 ,电解反应为 。
(2)X为Cu,Y为Fe,Z为CuSO4时,阳极反应为 ,阴极反应为 。
如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。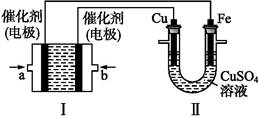
(1)a处应通入 (填“CH4”或“O2”),b处电极上发生的电极反应式是 ;
(2)电镀结束后,装置Ⅰ中溶液的pH (填“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度 ;
(3)电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有 (忽略水解);
(4)在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8 g,则装置Ⅰ中理论上消耗甲烷 L(标准状况下)。
(1)据报道,科研人员新近开发出一种由甲醇和氧气以及强碱作电解质溶液的新型电池,可供手机连续使用一个月。据此请回答以下问题:
①甲醇是 极,电极反应是 。
②电池反应的离子方程式是 。
(2)一般说来,根据一个氧化还原反应便可设计一个原电池。例如,某种燃料电池的总反应是CH4+2O2+2OH- C+3H2O。在此燃料电池中,通CH4极是 极,通O2极是 极,每消耗1 mol CH4,转移电子 mol,此电池的电解质溶液为 ,负极发生的电极反应是 ,正极发生的电极反应是 。
C+3H2O。在此燃料电池中,通CH4极是 极,通O2极是 极,每消耗1 mol CH4,转移电子 mol,此电池的电解质溶液为 ,负极发生的电极反应是 ,正极发生的电极反应是 。
全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。如图是钒电池基本工作原理示意图: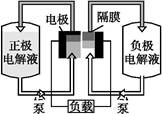
请回答下列问题:
(1)硫酸在电池技术和实验室中具有广泛的应用,在传统的铜锌原电池中,硫酸是 ,实验室中配制硫酸亚铁时需要加入少量硫酸,硫酸的作用是 。
(2)钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、V)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O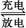 +V+2H+。放电时的正极反应式为 ,充电时的阴极反应式为 。放电过程中,电解液的pH (选填“升高”“降低”或“不变”)。
+V+2H+。放电时的正极反应式为 ,充电时的阴极反应式为 。放电过程中,电解液的pH (选填“升高”“降低”或“不变”)。
(3)钒电池基本工作原理示意图中“正极电解液”可能是 。
a.V、VO2+混合液
b.V3+、V2+混合液
c.V溶液
d.VO2+溶液
e.V3+溶液
f.V2+溶液
(4)能够通过钒电池基本工作原理示意图中“隔膜”的离子是 。