在含n mol FeBr2的溶液中,通入Cl2,有x mol Cl2发生反应。
(已知:还原性:Fe2+>Br—)
(1)当x≤ 时,反应的离子方程式为: 。
时,反应的离子方程式为: 。
(2)当反应的离子方程式为:2Fe2++4Br -+3Cl2=2Fe3++2Br2+6Cl-时,x与n的关系为 。
在下列各组气体中,试分析判断哪种气体更易液化?
①Cl2、N2;②SiH4、CH4;③SO2、CO2;④邻二甲苯、对二甲苯;⑤甲烷、乙烷;⑥丁烷、异丁烷
已知M2+3d轨道上有5个电子,试推出:
(1)M原子的核外电子排布。
(2)M原子的最外层和最高能级组中电子数各为多少?
(3)M元素在周期表中的位置。
由下列元素在周期表中的位置,写出元素原子的价电子排布式。
(1)第4周期ⅥB族;
(2)第5周期ⅠB族;
(3)第5周期ⅣA族;
(4)第6周期ⅡA族;
(5)第4周期ⅦA族。
铁及其化合物之间的相互转化可用下式表示: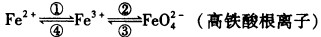
回答下列有关问题:
(1)铁元素位于元素周期表的第四周期第Ⅷ族,原子序数是26,最外层有2个电子。元素铁的原子结构示意图是。
(2)检验硫酸铁溶液中是否存在Fe2+的方法是
(3)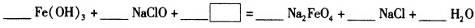
(4)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为Fe3+。Na2FeO4之所以能净水,除了能消毒杀菌外,另一个原因是(结合离子方程式说明) 。
钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用。
(1)Mg—H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,结构如图所示。电池工作时,正极的电极反应式 。常温下,用该电池电解200mL的饱和硫酸铜溶液(电极为惰性电极),反应时溶液中水的电离平衡移动(填“向左”“向右”或“不”);当消耗24mg金属Mg,电解后溶液的pH=(不考虑溶液的体积变化)。
(2)利用电解法在铁制品上镀铜可以防止铁被腐蚀,以下说法正确的是。
a.电镀时,铜和石墨都可以做阳极,可溶性铜盐作电解质溶液
b.电镀过程中,温度升高,电解反应速率加快
c.电镀过程中,电能全部转化为化学能
d.电镀过程中,铜离子向阴极移动,发生还原反应
(3)NaHS可作为沉淀剂除去溶液中的Cu2+。常温下,NaHS溶液显碱性,原因是(用离子方程式和必要的文字说明)。向含有Cu2+的废水中加入少量NaHS固体,废水溶液的pH(填“增大”“减小”或“不变”)。