下图中每一方框中的字母代表一种反应物或生成物。已知:A、B、C、D均为前三周期元素的单质,也是中学化学教材中常见的物质。其中A、B为固体,且B是良好的半导体材料,C、D为气体,电解H的饱和溶液生成x、C和D,此反应是一个重要的化工反应(物质间相互转化时参加反应或生成的H2O已略去)
(1)B单质为 .列举B的氧化物的一种重要的工业用途为 。
(2)X的电子式为 ,Y是(填化学式) 。
(3)E和G在水溶液中混合反应,其离子反应方程式为
。
若在E的水溶液中通入过量的CO2,其离子反应方程式为
。
(4)25℃时用石墨电极电解含0.2 mol H的水溶液,在阳极产生0.2 mol气体时,测得此时溶液的体积为200 mL,则该溶液中C(OH-)最接近的数值为 。
化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质。完成下列有关方程式。
(1)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO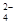 ,常用作脱氯剂,该反应的离子方程式为____________________________________________;
,常用作脱氯剂,该反应的离子方程式为____________________________________________;
(2)酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:__________________________。
(3)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:_______________、_____________________。
(4)向含有n mol 溴化亚铁的溶液中通入等物质的量的的氯气,请写出离子方程式:____________________。
下表是元素周期表的一部分。
已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):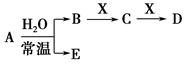
(1)⑧的元素符号是________。
(2)⑤与As两种元素中,非金属性较强的是________(填元素符号)。
(3)若E为氧化物,则A、X的化学式分别为________、________。
(4)Y由②⑥⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂。As可与Y的碱性溶液反应,当消耗1 mol还原剂时,消耗2.5 mol氧化剂,转移5 mol电子。该反应的离子方程式为______________________。
已知铜和浓硫酸可以在加热条件下发生反应,化学方程式如下(已配平):
Cu+2H2SO4(浓) CuSO4+A↑+2H2O
试通过计算和推理完成下面的问题:
(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为 。A物质可以与强碱反应生成盐和水。则A应该属于 (用字母代号填写)。
a.酸
b.碱
c.盐
d.酸性氧化物
e.碱性氧化物
(2)一定量的铜片与含1.8mol H2SO4的浓H2SO4充分反应(浓H2SO4过量),如果该反应过程中转移了0.2 mol电子,生成的CuSO4的质量为 g,生成的A气体在标准状况下体积为 L(假设气体全部逸出)。
(3)将(2)中反应后所得到的溶液稀释后与足量Ba(OH)2溶液反应,所得沉淀的质量为 g。写出此过程中发生反应的离子方程式:
,
。
实验室要配制0.1mol/L的稀硫酸980mL,回答下列问题:
(1)需要98%密度为1.84g/cm3的浓硫酸 ______ mL
(2)配制时,必须使用的仪器有______(填代号)还缺少的仪器是______、______。
①烧杯 ②10 mL量筒③20 mL量筒 ④托盘天平(带砝码) ⑤玻璃棒
(3)配制时,该实验两次用到玻璃棒,其作用分别是______、______。
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不影响”)
①用量筒量取98%的硫酸时俯视。()
②如果加水超过了刻度线,取出水使液面恰好到刻度线。()
③容量瓶没有干燥。()
近年来,我国对储氢纳米碳管的研究获得了重大进展,电弧法合成的纳米碳管常伴有大量物质——碳纳米颗粒。这种碳纳米颗粒可用氧化法提纯。其反应的化学方程式为:
C + K2Cr2O7+ H2SO4(稀)="=" CO2+ K2SO4+ Cr2(SO4)3+
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂是 ,氧化产物是 。
(3)H2SO4在上述反应中表现出来的性质是 。
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
(4)上述反应中若产生11.2 L(标准状况下)的气体物质,则转移的电子数目为 。