据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是( )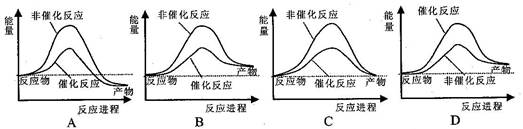
下列说法中不正确的是()
| A.若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子 |
| B.C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键 |
| C.同周期ⅠA族元素和 ⅦA族元素之间只能形成离子化合物 |
| D.由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键 |
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是()
| A.弱酸溶液和强碱溶液反应 | B.生成了一种强酸弱碱盐 |
| C.强酸溶液和弱碱溶液反应 | D.一元强酸溶液和一元强碱溶液反应 |
①14Cu2++5FeS2+12H2O = 7Cu2S + 5Fe2+ + 24H++3SO42-
②Mn2+ + S2O82- + H2O— MnO4- + SO42-+ H+对上述两个反应判断正确的是( )
| A.①②反应中SO42—都是氧化产物 | B.两个反应中电子转移数目都是10mol |
| C.①反应中的硫元素既被氧化又被还原 | D.氧化性:S2O82—>MnO4— |
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是( )
| A.a点发生反应的离子方程式是: Al3++2SO42-+2Ba2++3OH— = Al(OH)3↓+2BaSO4↓ |
| B.b点消耗Ba(OH)2溶液体积为200mL |
| C.从a→b 、b→c点过程中发生反应的离子方程式依次为:NH4++OH-=NH3·H2O Al(OH)3+OH-=AlO2-+2H2O |
| D.沉淀的质量:a点>c点 |
若室温时,将pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度为( )
| A.10a+b-12 % | B.10a+b-14 % | C.1012-a-b % | D.1014-a-b % |