下列有关实验的说法正确的是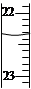
| A.测定溶液的pH时,应先将pH试纸润湿,然后进行检测 |
| B.滴定达终点时,右图滴定管的正确读数为23.65 mL |
| C.向AgI悬浊液中滴加少量NaCl溶液,沉淀转化为白色 |
| D.用已知浓度的盐酸滴定未知浓度的NaOH溶液时,锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 |
常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通入少量CO2气体生成HX和NaHCO3;往NaY溶液中通入少量CO2生成HY和Na2CO3。下列有关叙述正确的是 ()
| A.酸性由强至弱:HX>HY>H2CO3 |
| B.结合H+的能力:Y->CO32->X->HCO3- |
| C.溶液碱性:NaX>Na2CO3>NaY>NaHCO3 |
| D.NaX溶液中通入足量CO2后的离子浓度: c(Na+)>c(HCO3-)>c(X-)>c(OH-)>c(H+) |
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1 mol Cu2(OH)2CO3后恰好使电解液恢复到电解前的浓度和pH(不考虑CO2的溶解)。则电解过程中共转移电子的物质的量为 ( )。
| A.0.4 mol | B.0.5 mol |
| C.0.6 mol | D.0.8 mol |
用铅蓄电池电解甲、乙电解池中的溶液。已知铅蓄电池的总反应为:Pb+PbO2+2H2SO4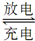 2PbSO4+2H2O。电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )
2PbSO4+2H2O。电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )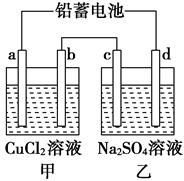
| A.d极为阴极 |
| B.放电时铅蓄电池负极的电极反应式为:PbO2+4H++SO42—+2e-===PbSO4+2H2O |
| C.若利用甲池精炼铜,b极应为粗铜 |
| D.若四个电极材料均为石墨,当析出6.4 g Cu时,两池中共产生标准状况下的气体3.36 L |
下列叙述正确的是( )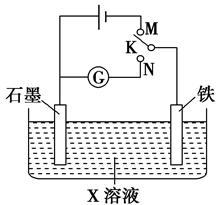
| A.K与N连接时,X为硫酸,一段时间后溶液的pH增大 |
| B.K与N连接时,X为氯化钠,石墨电极反应:2H++2e-===H2↑ |
| C.K与M连接时,X为硫酸,一段时间后溶液的pH增大 |
| D.K与M连接时,X为氯化钠,石墨电极反应:4OH--4e-===2H2O+O2↑ |
(2012年高考安徽卷)氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时:
①HF(aq)+OH-(aq)===F-(aq)+H2O(l) ΔH=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
在20 mL 0.1 mol·L-1氢氟酸中加入V mL 0.1 mol·L-1NaOH溶液。下列有关说法正确的是( )
| A.氢氟酸的电离方程式及热效应可表示为:HF(aq) F-(aq)+H+(aq) ΔH=+10.4 kJ·mol-1 |
| B.当V=20时,溶液中:c(OH-)=c(HF)+c(H+) |
| C.当V=20时,溶液中:c(F-)<c(Na+)=0.1 mol·L-1 |
| D.当V>0时,溶液中一定存在:c(Na+)>c(F-)>c(OH-)>c(H+) |