在室温时,向体积为V1、浓度为c1、pH=a的醋酸溶液中加入体积为V2、浓度为c2、pH=b的氢氧化钠溶液,充分反应。下列关于反应后混合液的叙述一定正确的是
| A.若pH=7,且V1=V2,则c1>c2 |
| B.若pH<7,则c(CH3COO-)>c(Na+)>c (H+)>c (OH-) |
| C.若cl=c2,且V1=V2,则a+b=14 |
| D.若pH>7,且V1=V2,则cl<c2 |
烟雾传感器中的放射源是241Am。已知Am的原子序数为95。下列关于241Am的说法正确的是
| A.241Am的中子数与电子数之差为146 |
| B.241Am与243Am的核外电子数相等 |
| C.241Am与243Am是同种核素 |
| D.241Am与243Am的化学性质不同 |
4月22日是世界地球日,我国今年的地球日主题为 :珍惜地球资源,转变发展方式,提高资源利用效益。下列有关做法与此不相符的是
| A.建立废旧电池回收站,对其进行回收再利用 |
| B.将木材边角料制成木屑颗粒,用作环保能源 |
| C.露天焚烧农作物秸秆还田,用作农作物肥料 |
| D.部分煤炭转直接开采为先在地下气化或液化 |
一定条件下,在体积为10L的固定容器中发生的反应:N2+3H2 2NH3,反应过程如下图所示,下列说法正确的是
2NH3,反应过程如下图所示,下列说法正确的是
| A.t1 min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间变化的关系 |
| C.0~8 min,H2的平均反应速率v(H2)=0.75 mol·L-1·min-1 |
| D.10~12 min,N2的平均反应速率为v(N2)=0.25mol·L-1·min-1 |
一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体总质量为49.6g,当其缓慢经过足量无水CaCl2时,无水CaCl2增重25.2g,则原混合气体中CO2的质量为
| A.12.5g | B.13.2g | C.19.7g | D.24.4g |
用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如下图,下列说法正确的是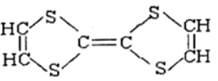
| A.该物质属于烃类 |
| B.该物质易溶于水 |
| C.该物质能使酸性高锰酸钾溶液褪色 |
| D.该物质是一种高分子化合物 |