定量分析中可用AgNO3溶液滴定Cl-溶液,加入K2CrO4为指示剂,达到滴定终点时溶液体积为50mL,c(Cl-) = 10-5 mol·L-1,AgNO3与CrO42- 生成砖红色的Ag2CrO4沉淀。已知Ksp(AgCl) = 1.77×10-10,Ksp(AgI) = 8.51×10-17,Ksp(Ag2CrO4) = 1.12×10-12,根据以上实验操作和有关数据,下列说法正确的是
| A.常温下,向含AgCl固体的AgCl溶液中加入NaCl固体,AgCl沉淀的量不变 |
| B.滴定终点时,溶液中CrO42-的浓度约为3.6×10-3 mol·L-1 |
| C.向10mL0.1moL/L AgNO3溶液中滴加3—5滴0.1moL/L NaCl溶液生成AgCl沉淀,再滴加KI溶液,生成AgI沉淀,能够说明Ksp(AgI)< Ksp(AgCl) |
| D.可用0.1 mol·L-1的KI溶液代替K2CrO4做指示剂 |
(4分)核磁共振氢谱(1HNMR)是研究有机物结构的有力手段之一。已知化合物分子结构中的等效氢原子(在化合物的结构中所处的环境相同的H原子)在1HNMR谱中会给出相同的峰(信号),峰的强度与H原子数成正比。例如:乙醛的结构中有①②两类氢原子且个数比为3:1,它在1HNMR谱中也有2个信号峰,其强度之比为3:l。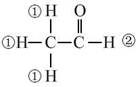
(1)若用乙醇进行核磁共振实验,所得核磁共振氢谱有______个峰,强度比为_________。
(2)某烃已知其相对分子质量为72,其分子式是______________,若要确定它的结构,我们对它核磁共振实验,发现氢谱有4个峰且强度比为6:1:2:3,则该烃的系统命名为______________。
下列实验方案合理的是
| A.向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体 |
| B.测定工业烧碱的含量(含杂质碳酸钠)可称取一定量样品放人锥形瓶中,加适量水溶解,再加入稍过量氯化钡溶液,用酚酞作指示剂,用标准浓度的盐酸滴定 |
| C.用分液漏斗分离苯与硝基苯 |
| D.除去氯化铁酸性溶液中的氯化亚铁:加入适量的硝酸溶液 |
在指定条件下一定能大量共存的离子组是()
| A.由水电离出的[OH-]=1×10-13mol/L的溶液中:Fe2+、NH4+、ClO-、Cl- |
| B.加入铝粉能放出氢气的溶液中:CO32-、AlO2-、I-、Na+ |
| C.能使蓝色石蕊试纸变红色的溶液中:Fe2+、NO3-、SCN-、SO42- |
| D.加入酚酞试液,呈无色的溶液中:NH4+、K+、SO42-、Al3+ |
从图中表示的各物质能量变化推断下列热化学方程式正确的(a、b均为正数)()
| A.4P(白磷) + 5O2(g) = 2P2O5(S) ; △H1= +(a+b) kJ/mol |
| B.4P(红磷) + 5O2(g) = 2P2O5(S) ; △H2= -(b)kJ/mol |
| C.4P + 5O2= 2P2O5(S) ; △H3= +(a+b) kJ/mol |
| D.P(白磷) = P(红磷) ; △H4= +(a)kJ/mol |
100℃时 PH=12的NaOH溶液与PH=2的硫酸溶液等体积混合,此温度下混合液的PH
A小于7B 大于7 C等于7 D无法判断