下列关于糖类的说法中,错误的是( )
| A.葡萄糖和果糖化学式(C6H12O6)相同,它们是同分异构体 |
| B.麦芽糖和蔗糖化学式(C12H22O11)相同,它们是同分异构体 |
| C.淀粉和纤维素化学式[(C6H10O5)n]相同,它们是同分异构体 |
| D.多糖可以水解成单糖,单糖不能再水解成更小的糖分子 |
下列物质之间的转化符合:“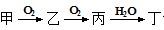 ”的组合是
”的组合是
①Na→NaOH;②Cu→Cu(OH)2;③S→H2SO4;④NH3→HNO3
| A.①②③ | B.①③④ | C.②③④ | D.全部 |
下列关于氯气的叙述中不正确的是
| A.可用向上排空气法收集少量的氯气 |
| B.与水反应生成的次氯酸是一种弱酸 |
| C.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
| D.与氢氧化钠溶液反应时,Cl2既被还原,同时又被氧化 |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.室温下,1L pH=1的盐酸中,由水电离的H+离子数目为0.1NA |
| B.标况下,11.2L SO3所含的分子数目为0.5 NA |
| C.甲烷碱性燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA |
| D.1 mol C2H6O分子中含有的O—H键数目一定为NA |
同温同压下,某容器充满O2重116 g,若充满CO2重122 g,现充满某气体重124 g,则某气体的相对分子质量为
| A.48 | B.28 | C.32 | D.4 |
纯碱和小苏打都是白色晶体,在日常生活中都可以找到。若要在家中将它们区分开来,下面的方法中可行的是
| A.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度 |
| B.分别用干净铁丝蘸取样品在煤气炉的火焰上灼烧,观察火焰颜色 |
| C.将样品溶解,分别加入澄清石灰水,观察是否有白色沉淀 |
| D.分别放在炒锅中加热,观察是否有残留物 |