设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.室温下,1L pH=1的盐酸中,由水电离的H+离子数目为0.1NA |
| B.标况下,11.2L SO3所含的分子数目为0.5 NA |
| C.甲烷碱性燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA |
| D.1 mol C2H6O分子中含有的O—H键数目一定为NA |
常温下,用0.1000 mol•L-1 NaOH溶液滴定 20.00 mL 0.1000 mol•L-1 CH3COOH溶液滴定曲线如上右图。下列说法正确的是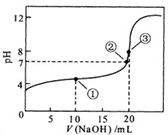
| A.点①所示溶液中:c(CH3COO-)+ c(OH-)= c(CH3COOH)+ c(H+) |
| B.点②所示溶液中:c(Na+)= c(CH3COOH)+ c(CH3COO-) |
| C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)] |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6 g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是
| A.原混合酸中HNO3的物质的量为0.1 mol |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+ = 3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e═Li2S+Fe ,有关该电池的下列中,正确的是
| A.Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价 |
| B.该电池的电池反应式为:2Li + FeS = Li2S + Fe |
| C.负极的电极反应式为Al-3e-=Al3+ |
| D.充电时,阴极发生的电极反应式为:Li2S + Fe -2e- = 2Li+ + FeS |
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列分析中正确的
| A.滴加KI溶液时,转移2mol e- 时生成1mol白色沉淀 |
| B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
| C.通入SO2时,SO2与I2反应,I2作还原剂 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
| A |
B |
C |
D |
|
| 实 验 |
用CCl4提取 溴水中的Br2 |
除去乙醇中的I2 |
加热分解MgCl2.6H2O得到纯净的MgCl2 |
配制100 mL 0.1000 mol·L-1 K2Cr2O7溶液 |
| 装 置 或 仪 器 |
 |
 |
 |
 |