X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的质子数是Y的核外电子数的一半,Y与M可形成化合物M2Y,下列说法正确的是
| A.Z元素的最高价氧化物的水化物的化学式为HZO4 |
| B.离子半径:M的离子>Z的离子>Y的离子>X的离子 |
| C.X、M两元素形成的化合物只有M2X、M2X2两种 |
| D.还原性:X的氢化物>Y的氢化物>Z的氢化物 |
设NA代表阿伏加德罗常数,下列说法正确的是
| A.用石墨电极电解Ca(NO3)2溶液,当转移电子数为0.2NA时,阴极析出4g金属 |
| B.常温下含有NA个NO2、N2O4分子的混合气,温度降至标准状况,其体积约为22.4L |
C.10g钾所含的电子数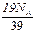 |
| D.0.1mol 24Mg32S晶体中所含中子总数为2.8NA |
下列各组离子一定能大量共存的是
| A.含有大量HCO3-的澄清透明溶液中:K+、C6H5O-、Cl-、Na+ |
| B.能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Fe2+ |
| C.常温下水电离出的c(H+)·c(OH-)=10-20的溶液中:Na+、ClO-、S2-、NH4+ |
| D.pH=7的溶液:Fe3+、Mg2+、SO42-、Cl- |
下列实验操作或对实验事实的叙述正确的是
①用酸性高锰酸钾溶液可以鉴别苯和甲苯
②如果皮肤上不慎沾有苯酚,应立即用酒精洗涤
③用pH试纸测得氯水的pH为2
④用稀硝酸清洗做过银镜反应实验的试管
⑤少量的钠、钾、白磷通常保存在煤油中
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物
| A.①③⑤ | B.①②④ | C.②④⑤ | D.②⑤⑥ |
化学与科学、技术、社会、环境密切相关。下列有关说法中不正确的是
| A.在我国上海举办的世博会采取了许多节能环保措施,充分利用太阳能是其中之一 |
| B.在食盐中加入适量的碘酸钾,是因为碘酸钾具有较强的氧化性,可抗人体老化 |
| C.煤的综合利用主要是通过煤的干馏、液化和气化,获得洁净的燃料和多种化工原料 |
| D.竹炭具有超强的吸附能力,能吸附新装修房屋内的所有有害气体 |
“促进低碳经济,减少CO2的排放”是联合国《哥本哈根气候变化》会议的主题。下列行为中不符合这一主题的是
| A.发展水电,开发新能源,如核能、太阳能、风能等,减少对化石能源的依赖 |
| B.限制化工发展,关停化工企业,消除污染源头 |
| C.推广利用微生物发酵技术,将植物桔杆、动物粪便等制成沼气以替代液化石油气 |
| D.推广煤的干馏、气化、液化技术,提供清洁、高效燃料和基础化工原料 |