(16分)止咳酮(F)具有止咳、祛痰作用。其生产合成路线如下: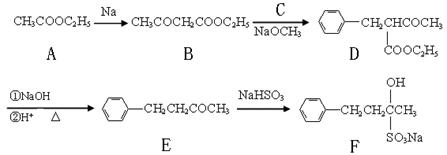
(1)写出B中含有的官能团名称: 。
(2)已知B→D反应属于取代反应,写出C(C属于氯代烃)的结构简式: 。
(3)写出E→F的反应类型: 。
(4)满足下列条件的E的同分异构体有 种。
①苯环上有两个邻位取代基; ②能与FeCl3溶液发生显色反应;
③除苯环外不含其它的环状结构。
(5)写出A→B的反应方程式: 。
(6)A→F六种物质中含有手性碳原子的是: (填物质代号)。
(7)目前我国用粮食发酵生产丙酮(CH3COCH3)占较大比重。利用题给相关信息,以淀粉为原料,合成丙酮。合成过程中无机试剂任选。
提示:合成路线流程图示例如下:
(1)如图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_______________。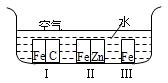
将1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在水槽里,放在光亮处。片刻后发现试管中气体颜色,试管中液面上升,试管壁上出现了,在该反应的所有产物中(HCl除外),常温下(填化学式)是气体,空间构型与甲烷完全相同的是(填化学式)。试写出甲烷与氯气反应生成一氯代物的化学反应方程式。
从能量转化的角度看,原电池是一种由_______能转变成________能的装置;用锌片、铜片和稀盐酸组成的原电池,负极是________,正极的电极反应是___________________,正极发生反应(填“氧化”或“还原”)
石油化工排放的废水中常含有多种还原性物质 。向水样中加入稍过量的重铬酸钾标准溶液,充分反应后,再用硫酸亚铁铵标准溶液滴定剩余的重铬酸钾,以检测石油化工废水中还原性物质的含量。
。向水样中加入稍过量的重铬酸钾标准溶液,充分反应后,再用硫酸亚铁铵标准溶液滴定剩余的重铬酸钾,以检测石油化工废水中还原性物质的含量。
⑴配制0.010mo1·L-1标准硫酸亚铁铵溶液500 mL时,需称取硫酸亚铁铵晶体[(NH4 )2Fe(SO4)2·6H2O]的质量为g。
)2Fe(SO4)2·6H2O]的质量为g。
⑵硫酸亚铁铵标准溶液在空气中放置后浓度会发生变化,需用重铬酸钾标准溶液标定硫酸亚铁铵溶液的实际浓度。现取0.0040 mo1·L-1重铬酸钾标准溶液10.00 mL,滴定时,用去25.00 mL硫酸亚铁铵溶液,则硫酸亚铁铵标准溶液的实际浓度为(K2Cr2O7的还原产物为Cr3+)。
⑶实际操作中,检测人员在标定标准硫酸亚铁铵溶液浓度时,每次取浓度值为c的重铬酸钾标准溶液10.0 mL,计算时只要测出滴定中消耗的标准硫酸亚铁铵溶液的体积(V,单位mL)就可以依据一个简单的计算式直接计算出标准硫酸亚铁铵溶液的实际浓度。该计算式为。
学校化学实验室一试剂瓶标签严重破损,只能隐约看到一些信息,如图所示。
(1)该物质(M)分子式为:;
(2)A与M互为同分异构体,B无支链,B与羧酸和醇都能发生酯化反应,A在一定条件下能发生如下转化: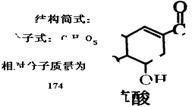

C与F互为同系物,H能使Br2/CCl4溶液褪色,H物质得到的1H-NMR谱中有5个吸收峰。
①A的结构简式为 。
。
②写出一个证明E中官能团的化学方程式 ,反应类型 ;
,反应类型 ;
写出C与D反应生成高聚物的化学方程式,
③写出与H官能团种类和数目都相同的同分异构体任意两个: