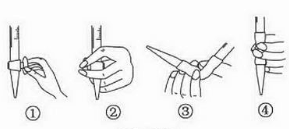
某课外活动小组为了测定某氯化锶(SrCl2)样品的纯度,设计了如下方案:
称取1.0g样品溶解于适量水中,向其中加入含AgNO32.38g的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应生成沉淀的离子),Cl―即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。请回答下列问题:
(1)滴定反应达到终点的现象是 ;
(2)实施滴定的溶液以呈 (选填“酸性”、“中性”或“碱性”)为宜,加
(填化学式)试剂可达到这一目的;
(3)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n (Clˉ)的测定结果 (选填“偏高”、“偏低”或“无影响”);
(4)到达终点后,则必须轻轻摇动锥形瓶,(此时不得剧烈摇动)以减少误差,否则这种误差会使n (Clˉ)测定值偏低,这说明两者的溶解度:AgCl AgSCN(填“>”或“<”);
(5)若以Fe3+的溶液作指示剂,用NH4SCN标准溶液滴定剩余的AgNO3时,用去上述浓度的NH4SCN溶液20.0mL,则原氯化锶样品的纯度为 。
(9分)
(1)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如下图所示。从图中可以看出,该同学在操作时的一个错误是_________,烧杯的实际质量为___________g。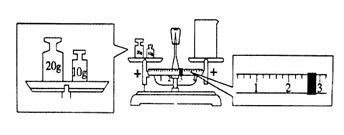
(2)指出下面三个实验中各存在的一个错误: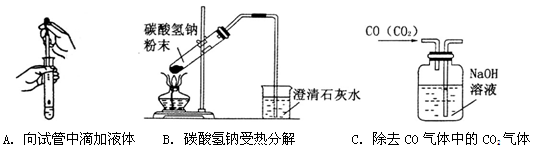
A.__________________________________________________________________________;
B._________________________________________________________________________;
C.__________________________________________________________________________。
(10分)工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)===Na2SO3(aq)+H2S(aq)(Ⅰ)
2H2S(aq)+SO2(g)===3S(s)+2H2O(l)(Ⅱ)
S(s)+Na2SO3(aq)Na2S2O3(aq)(Ⅲ)
已知Na2S2O3·5H2O遇酸易分解:S2O+2H+===S↓+SO2↑+H2O供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液。
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若________________,则整个装置气密性良好。装置D的作用是__________。装置E中为________溶液。
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择________。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是__________________。反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有________。
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(3)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为________。
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:________________________________________。
(11分)硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。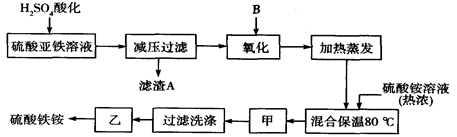
请回答下列问题:
(1)操作甲、乙的名称分别是:甲______________,乙___________________。
(2)下列物质中最适合的氧化剂B是;使用过程中分多次添加适量的氧化剂原因是
a.NaClO b.H2O2 c.KMnO4d.K2Cr2O7
(3)上述流程中,用足量最适合的氧化剂B氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,所加试剂为(写名称)。能否用酸性的KMnO4溶液?理由是:。(可用文字或方程式说明)
(4)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba (NO3)2溶液,恰好完全反应。则该硫酸铁铵的化学式为________________(写出计算过程)
某学生为了测定部分变质的Na2SO3样品的纯度,设计了如下实验,回答下列问题:
(1)写出A装置中玻璃仪器的名称:酒精灯、______、。
(2)实验开始后,写出B中反应的离子方程式_______________________。
(3)C中的现象是______________,E装置的作用是_____________________。
(4)某学生按下图所示称取一定量的Na2SO3样品放入A装置的烧瓶中,滴入足量的H2SO4完全反应。然后将B中完全反应后的溶液与足量的BaCl2溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g。请你计算原样品中Na2SO3的纯度为________(精确到0.1%)。
(5)在过滤沉淀时若滤液出现浑浊,则必须要重复操作,若该学生没有重复过滤,则测定的结果将______(填“偏高”、“偏低”或“无影响”)。
(6)要使测定结果准确,第一:装置气密性必须良好;第二:应先点燃___处酒精灯(填装置字母)。
碘元素的单质和化合物在现实生产生活中应用广泛。
(1)碘化钾(KI)是常用的还原剂。某研究性学习小组利用碘酸钾(KIO3)测定碘化钾的浓度。在10.00mL的KI溶液中逐滴滴入用硫酸酸化的KIO3溶液,溶液颜色不再变化后,用Na2S2O3溶液滴定生成的I2(使用淀粉做指示剂),消耗0.2000mol·L-1 Na2S2O3溶液30.00mL。
滴定过程发生的离子方程式如下:2S2O32-+I2===S4O62-+2I-;
①写出本实验中碘酸钾和碘化钾反应的化学方程式,并标出电子转移的方向和数目:_______________________________________________________。
②滴定终点判断;
③测定的KI溶液浓度是mol·L-1。
(2)探究酸性KIO3溶液的与KI溶液反应中KIO3浓度和温度对反应速率的影响,生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。
某同学设计实验如下表所示: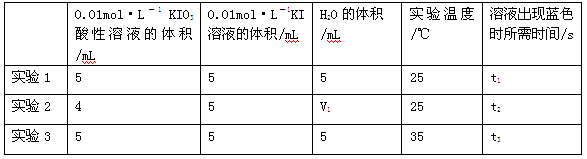
①由小到大比较t1、t2、t3的大小;表中V1=mL;
②用Na2S2O3标准溶液滴定生成的I2,滴定前排气泡时,应选用下图中的_________。