(共9分)(1)现有A、B、C、D、E五种元素,A的原子核中没有中子;B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;5.4 g D的单质跟足量盐酸反应,生成D3+和6.72 L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同电子层结构。
①写出元素符号:
A ,C ,E 。
②B、D的最高价氧化物对应水化物相互反应的离子方程式为:
③用电子式表示C与E形成E2C的过程: 。
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质。右图是元素周期表的一部分。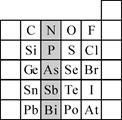
①根据元素周期律,预测:酸性强弱 H3AsO4 H3PO4。(用“>”或“<”表示)
②元素S的最高正价和最低负价的代数和为____________,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度 。(选填“更大”、“更小”或“相同”)
③Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是________________________________________________。
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<” )。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<” )
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积。(填“ >” 或“=”或“<” )
根据下列叙述写出相应的热化学方程式:
(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是
_____________________________________。
(2)下图是SO2生成SO3反应过程中能量变化的曲线图。该反应的热化学方程式为: 。
某温度(T ℃)下的溶液中,c(H+)=10-x mol·L-1,c(OH-)=10-y mol·L-1,x与y的关系如图所示,请回答下列问题:
(1)此温度下,水的离子积Kw为________,则该温度T______25(填“>”、“<”或“=”)。
(2)在此温度下,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示。
| 实验序号 |
Ba(OH)2溶液的体积/mL |
盐酸的体积/mL |
溶液的pH |
| ① |
22.00 |
0.00 |
8 |
| ② |
22.00 |
18.00 |
7 |
| ③ |
22.00 |
22.00 |
6 |
假设溶液混合前后的体积变化忽略不计,则a=________,实验②中由水电离产生的c(OH-)=______mol·L-1。
(3)在此温度下,将0.1 mol·L-1的NaHSO4溶液与0.1 mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
| 甲 |
乙 |
丙 |
丁 |
|
| 0.1 mol·L-1 Ba(OH)2溶液体积/mL |
10 |
10 |
10 |
10 |
| 0.1 mol·L-1 NaHSO4溶液体积/mL |
5 |
10 |
15 |
20 |
①按丁方式混合后,所得溶液显________(填“酸”、“碱”或“中”)性。
②写出按乙方式混合后,反应的离子方程式:________________________。
③按甲方式混合后,所得溶液的pH为__________。
⑴有下列四种溶液:①100mL 0.1mol/L H2SO4溶液;②100mL 0.15mol/L HCl溶液 ③100mL 0.2mol/L CH3COOH溶液;④200mL 0.1mol/L CH3COOH溶液。
其中pH最小的是 (填序号,下同),由水电离的H+浓度最大的是 ,与足量的Zn反应,生成H2最少的是 ;①和③分别与100mL 0.2mol/L NaOH溶液反应,放出热量少的是 ,理由是 。
⑵实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。该学生取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定。滴定达到终点的标志是 ;在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(填字母序号)。
| A.滴定终点读数时俯视 |
| B.酸式滴定管使用前,水洗后未用待测盐酸润洗 |
| C.锥形瓶水洗后未干燥 |
| D.称量NaOH固体中混有Na2CO3固体 |
E.碱式滴定管尖嘴部分有气泡,滴定后消失
Ⅰ.某反应为:4CuI + Hg = Cu2HgI4 + 2Cu (反应前后的I均为-1价),试回答:
①上述反应产物Cu2HgI4中,Hg元素显 价;
②CuI发生 反应(填氧化或还原)。
Ⅱ.某反应为:3H2O2+Cr2(SO4)3 +10KOH = 2K2CrO4 + 3K2SO4 + 8H2O
①反应中氧化剂是 (填化学式),被氧化的元素 (填元素符号);
②用单线桥表示出该反应中电子转移的方向和数目(在答题卡上完成)。
Ⅲ.有下列三个反应:
A. 2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2
B. 2FeCl2 + Cl2 = 2FeCl3
C. 2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
①上述三个反应中氧化剂氧化性强弱关系为 ;
②在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是 。