实验室配制100g 10%的氯化钠溶液,请按要求回答问题。
(1)量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g的砝码,则天平上的游码位置应是图中的__ __ (填字母)。 
(2)下列仪器中,量取水时需要用到d和____仪器,溶解时需要用到e和___仪器。
a.烧杯 b.10mL量筒 c.100mL量筒 d.滴管 e.玻璃棒 f.药匙 g.蒸发皿
(3)在粗盐提纯中,将氯化钠溶液蒸发至有较多量固体析出后,应 ,并用玻棒不断搅拌,利用余热将余下溶液蒸发至干。
(4)实验室中配好的溶液,应贴上标签密封放到试剂柜中保存。一定溶质质量分数的氯化钠溶液须密封保存的原因是________。
有下列物质:
| A.红磷 | B.氮气 |
| C.铜绿 | D.碳酸氢铵 |
E.金刚石 F. 二氧化碳,选择合适的物质,将其序号填入下列对应的空格中:
(1)一种常见的化肥,受热易分解____________;
(2)光合作用的原料之一____________;
(3)绿色固体,加热变成黑色_____________;
(4)自然界中最硬的物质,可以用来划玻璃______________;
(5)燃烧产生大量白烟,可以用来制造烟幕弹_____________;
(6)可以充到食品包装袋里做保护气的是____________。
下列事实说明空气中含有哪些成分:
(1)蜡烛在空气中可以燃烧,说明空气中含有 。
(2)在空气中盛有冰水的杯子外壁会出现水珠,说明空气中含有 。
(3)澄清石灰水长期露置空气中,表面出现一层白膜,说明空气中含有 。
(4)空气可以用作制取氮肥的原料,说明空气中含有____________。
写出下列实验所需仪器的名称:
(1)量取一定体积的液体需用 ;
(2)用作收集或贮存少量气体时需用 ;
(3)吸取和滴加少量液体用 ;
(4)过滤时制作过滤器需要 和滤纸;
(5)做镁条燃烧实验时夹持镁带的仪器是_____________,为防止烫坏实验桌面,需要用______________。
通过你的学习,你已经掌握了实验室制取气体的有关规律,请结合下图回答问题: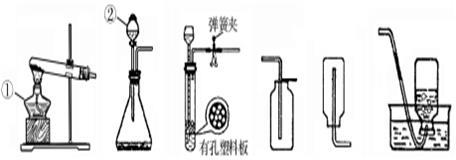
A B C D E F
(1)写出图中标号仪器的名称① ② 。
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置和收集装置是 (填字母编号);反应文字表达式为 。
(3)用加热高锰酸钾的方法制取氧气并用排水法收集,有以下操作步骤:(1)加热;(2)连接好装置;(3)停止加热;(4)移开导气管;(5)装入药品并固定在铁架台上;(6)检查装置的气密性;(7)收集气体。其中正确的操作
| A.(2)(6)(5)(1)(7)(3)(4) |
| B.(2)(6)(5)(1)(7)(4)(3) |
| C.(6)(2)(5)(1)(7)(4)(3) |
| D.(2)(6)(1)(5)(7)(3)(4) |
装入高锰酸钾后应在试管口塞一团棉花,其目的是
(4)用B装置通过分解反应制取氧气,则②中装的液体药品是 ;
在X2Y和YZ2中,Y的质量分数分别为40%和50%,则X2YZ3中Y的质量分数为 。