铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢。K2Cr2O7和CrO3大量用于鞣革、印染、颜料、电镀等工业中,是工业上造成铬污染的主要原因。近期暴光的“毒胶囊”事件中,就是因为用工业皮革的下脚料或破皮鞋等为原料制成的工业明胶被冒充成食用明胶制成胶囊,造成胶囊内的铬严重超标。
(1)CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。 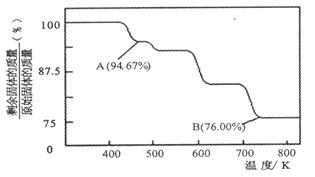
①A 点时剩余固体的成分是 (填化学式)。
②从开始加热到 750K 时总反应方程式为 。
(2)Cr(Ⅵ)主要以CrO42-和Cr2O72-形态存在,在酸性条件下具有很强的氧化性,它们在溶液中存在如下转化:CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O;K=4.2×1014。若要使溶液由黄色变橙色,则应采取的措施是 。
Cr2O72-(橙色)+H2O;K=4.2×1014。若要使溶液由黄色变橙色,则应采取的措施是 。
| A.加NaOH | B.加盐酸 | C.加硫酸 | D.加AgNO3 |
(3)工业废水中常含有一定量的Cr(Ⅵ),毒性较大,它们会对人类及生态系统产生很大损害。净化处理方法之一是将含Cr2O72-的废水放入电解槽内,用铁作阳极,加入适量的NaCl进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀以除去[已知KspFe(OH)3=4.0×10-38,KspCr(OH)3=6.0×10-31]。
①电解过程中 NaCl 的作用是 。
②写出阳极的电极反应式 。
③写出Fe2+和Cr2O72-发生反应生成Fe3+和Cr3+的离子反应方程式 。
④已知电解后的溶液中c(Fe3+)=2.0×10-13 mol·L-1,则溶液中c(Cr3+)为 mol·L-1。
已知有下图所示物质相互转换关系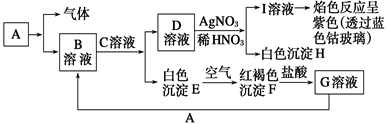
试回答:
(1)写出B的化学式,D的化学式。
(2) 写出由E转变成F的现象;其发生反应的化学方程式________。
写出由E转变成F的现象;其发生反应的化学方程式________。
(3)鉴别B溶液中阳离子的操作方法及实验现象__________________;
(4)向G溶液中加入A的离子方程式________
有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO、CO中的一种或几种,取此溶液做下列实验:①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气 体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断:
体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断: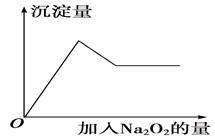
(1)溶液中一定含有的离子是______________ 。
。
(2)溶液中肯定不含有的离子是_______________ _。
_。
(3)可能含有的离子是____________。
A 、B、C、D是四种可溶性化合物,分别由阳离子K+、Ba2+.、Al3+、 Fe3+和阴离子OH—、CO
、B、C、D是四种可溶性化合物,分别由阳离子K+、Ba2+.、Al3+、 Fe3+和阴离子OH—、CO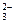 、NO
、NO 、SO
、SO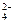 两两组合而成,它们的溶液能发生如下反应:
两两组合而成,它们的溶液能发生如下反应:
(1)A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失。
(2)C与D反应生成有色沉淀。
(3)B与C反应生成白色沉淀。
写出它们的化学式:
A._________;B._________;C._________;D._________;
下图为中学化学中常见物质的转化关系,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物,试推断:
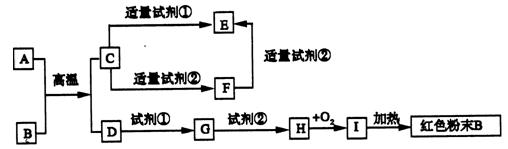
(1)写 出物质的化学式:
出物质的化学式:
(2)写出下列反应的方程式:
C →F的离子方程式:_____________________________________________
→F的离子方程式:_____________________________________________
H→I的化学方程式:______________________________________________
(1) 同期表中位于第8纵行的铁元素属于第________族;
(2) 同期表中最活泼非金属元素位于第________纵行;
(3) 所含元素超过18种的周期是第________、________周期。