下列热化学方程式中,△H能正确表示物质的燃烧热的是
| A.C(s) +1/2O2(g) ="=CO(g);" △H=-110.5 kJ/mol |
| B.CO(g) +1/2O2(g) ==CO2(g); △H=-283.0 kJ/mol |
| C.H2(g) +1/2O2(g)==H2O(g); △H=-241.8 kJ/mol |
| D.2C8H18(l) +25O2(g)==16CO2(g)+18H2O(l); △H=-11036 kJ/mol |
下列有关浓H2SO4性质的叙述中,错误的是()
| A.浓硫酸具有脱水性,因而能使蔗糖炭化 |
B.在反应HCOOH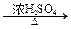 CO↑+H2O中,浓H2SO4只表现脱水性 CO↑+H2O中,浓H2SO4只表现脱水性 |
C.在反应Cu+2H2SO4(浓)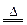 CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 |
| D.浓硫酸具有吸水性,因而能使CuSO4·5H2O转化为CuSO4 |
下列说法正确的是()
| A.ⅠA族元素的金属性一定比ⅡA族元素的金属性强 |
| B.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C.同主族元素单质的熔沸点从上到下逐渐升高 |
| D.第三周期元素的离子半径,从左到右逐渐减小 |
在F、P、S三种元素中,每种元素都有某些方面区别于其他两种元素;若从中选出氟元素,选择的理由是()
| A.单质与冷水反应非常剧烈 | B.单质固态时属于分子晶体 |
| C.一定条件下,能与氢气发生化合反应 | D.最高价氧化物对应的水化物是强酸 |
下列性质中,可以证明某化合物内一定存在离子键的是()
| A.晶体可溶于水 | B.具有较高的熔点 |
| C.水溶液能导电 | D.熔融状态能导电 |
下列各分子中,所有原子都满足最外电子层上有8电子的结构的是()
| A.H2O | B.PCl3 | C.SO2 | D.BF3 |