原电池是化学对人类的一项重大贡献。
(1)某兴趣小组为研究原电池原理,设计如图装置。
①a和b不连接时,烧杯中发生反应的离子方程式是__________。
②a和b用导线连接,Cu极为原电池__________极(填“正”或“负”),电极反应式是__________。Zn极发生__________(填“氧化”或“还原”)反应。溶液中H+移向__________(填“Cu”或“Zn”)极。
③无论a和b是否连接,Zn片均被腐蚀。若转移了0.2mol电子,则理论上Zn片质量减轻了__________g。
(2)有同学想把Ba(OH)2•8H2O晶体与NH4Cl晶体的反应设计成原电池,你认为是否可行?________(填“是”或“否”),理由是__________。
(17分)下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:。装置B中饱和食盐水的作用是;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入。
| a |
b |
c |
d |
|
| Ⅰ |
干燥的有色布条 |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
| Ⅱ |
碱石灰 |
硅胶 |
浓硫酸 |
无水氯化钙 |
| Ⅲ |
湿润的有色布条 |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为色,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:。
(5)如果将过量二氧化锰与20 mL 12 mol·L-1的浓盐酸混合加热,充分反应后生成的氯气0.06 mol。(填“大于”“小于”“等于”),若有17.4 g的MnO2被还原,则被氧化的HCl的质量为。
过氧化钠保存不当容易变质,生成Na2CO3。
(1)某过氧化钠样品已经部分变质,请你设计实验,限用一种溶液,证明过氧化钠已经变质
(2)检验样品中还有过氧化钠的方法是
(3)某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。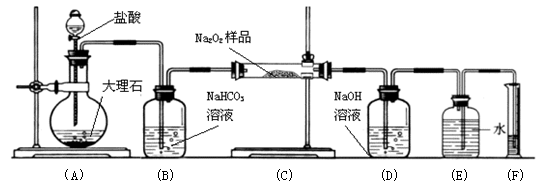
上图中的E和F构成量气装置,用来测定O2的体积。
①写出装置A和B中发生反应的离子方程式:
装置A:
装置B:
②NaOH的作用是
③他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
下列实验操作完全正确的是
| 编号 |
实验 |
操作 |
| A |
钠与水的反应 |
用镊子从煤油中取出金属钠,切下绿豆大小,放入装满水的烧杯中 |
| B |
配制一定浓度的氯化钾溶液500 mL |
准确称取氯化钾固体,放入到500 mL的容量瓶中,加水溶解、振荡、摇匀、定容 |
| C |
闻氯气的方法 |
用手轻轻地在瓶口扇动,使极少量氯气飘进鼻孔 |
 D D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个烧杯,上层液体继续从分液漏斗下端管口放出 |
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL 稀H2SO4溶液;以0.14mol/L的NaOH溶液滴定上述稀 H2SO425mL,滴定终止时消耗NaOH溶液15mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
| A.用酸式滴定管取稀H2SO4 25 mL,注入锥形瓶中,加入指示剂。 |
| B.用待测的溶液润洗酸式滴定管。 |
| C.用蒸馏水洗干净滴定管。 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 |
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写):。
②该滴定操作中应选用的指示剂是:。
③在G操作中如何确定终点?。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”)。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度为mol/L (计算结果保留两位小数)
(14分)某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如下:
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
III.按如图所示装置连接仪器、检查气密性、装入化学试剂。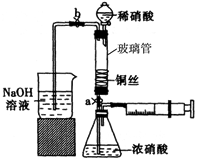
(1)过程I发生反应的离子方程式是。
(2)写出过程III中检查气密性的方法。
(3)过程III的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是,一段时间后使反应停止的操作是,关闭a,取下注射器。
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生。稀硝酸充满玻璃管的实验目是,该反应的离子方程式是。
(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):
| 实验编号 |
水温/℃ |
液面上升高度 |
| 1 |
25 |
超过试管的2/3 |
| 2 |
50 |
不足试管的2/3 |
| 3 |
0 |
液面上升超过实验1 |
①根据上表得出的结论是温度越(填“高”或“低”),进入试管中的溶液越多。
②查阅资料:a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2 3HNO2 =HNO3+2NO+H2O;
b.HNO2不稳定。
则产生上述现象的原因是。