已知:2Zn(s)+O2(g)=2ZnO(s) △H=-701.0kJ·mol-1
2Hg(l)+O2(g)=2HgO(s) △H=-181.6kJ·mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l)的△H为
| A.-259.7 kJ·mol-1 | B.-519.4kJ·mol-1 |
| C.+259.7 kJ·mol-1 | D.+519.4kJ·mol-1 |
下列溶液中的氯离子浓度与50 mL 1 mol /L的AlCl3溶液中氯离子浓度相等的
| A.150 mL 2 mol /L的KCl | B.75 mL 2 mol /L的CaCl2 |
| C.150 mL 1 mol /L的NaCl | D.75 mL 3 mol /L的NH4Cl |
某溶液由NaCl、MgCl2、Al2(SO4)3、Na2SO4组成,已知c(Na+)=0.4mol/L,c(Al3+)="0.2" mol/L,c(Mg2+)=0.1mol/L,c(Cl-)=0.3mol/L则SO42-的物质的量浓度为
| A.0.3 mol/L | B.0.4mol/L | C.0.45mol/L | D.0.55mol/L |
相对分子质量为M的某物质,在室温下溶解度为S g,此时测得该物质饱和溶液的密度为ρg/cm3,则该饱和溶液的物质的量的浓度是
A.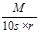 mol/L mol/L |
B.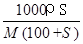 mol/L mol/L |
C.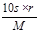 mol/L mol/L |
D.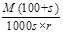 mol/L mol/L |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.48克O2和O3的混合物含有氧原子数3NA |
| B.22.4L甲烷(CH4)所含的原子数为5NA |
| C.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为 NA |
| D.在20℃,1.01×105Pa(即非标准状况)时,11.2L氧气所含的原子数为NA |
下列叙述正确的是
| A.1 molMg2+的质量为24g/mol |
| B.0.5mol CH4中含有3.01×1023个电子 |
| C.3.01×1023个SO2分子的质量为32g |
| D.CH4的摩尔质量为16g |