将稀硝酸与稀氨水混合,不可能出现的结果是()
| A.pH=7,且c(NH4+)=c(NO3-)>c(H+)=c(OH-) |
| B.pH<7,且c(NO3-)+c(OH-)=c(H+)+c(NH4+) |
| C.pH<7,且c(H+)>c(NO3-)>c(OH-)>c(NH4+) |
| D.pH>7,且c(NH4+)>c(OH-)>c(NO3-)>c(H+) |
下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是()
| A.NaClO 溶液中通入过量SO2 ClO -+SO2 + H2O ="=" HClO + HS03– |
| B.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应 CH3OH+H2O-6e-=CO2↑+6H+ |
| C.AlCl3溶液中投入过量Na:Al3+ + 4Na+2H2O ==AlO2 -+4Na+ + 2H2 ↑ |
| D.向明矾溶液中滴加Ba(OH)2,恰好使SO42- 沉淀完全: |
2Al3++3S04 2-+ 3Ba2+ + 6OH - ="=" 2Al(OH)3↓+ 3BaSO4↓
近年来用合成方法制备了多种新奇的有机物,例如分子具有如下图所示立体结构的环状化合物:
有人认为上述有机物中①立方烷、棱晶烷可以看做是烷烃的同系物;②盆烯是乙烯的同系物;③棱晶烷、盆烯是苯的同分异构体。上述看法中正确的是()
| A.②③ | B.除①都正确 | C.只有① | D.只有③ |
从下列事实所得出的相应结论正确的是()
| 实验事实 |
结论 |
|
| ① |
 的水溶液可以导电 的水溶液可以导电 |
 是电解质 是电解质 |
| ② |
将 通入到 通入到 溶液中产生白色浑浊 溶液中产生白色浑浊 |
酸性: |
| ③ |
 溶液与 溶液与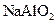 溶液混合产生白色沉淀 溶液混合产生白色沉淀 |
酸性: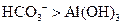 |
| ④ |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性: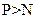 |
| ⑤ |
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 |
该溶液一定有 NH4+ |
| A.③④⑤ | B.②③⑤ | C.①②③ | D.全部 |
在密闭容器中,反应X2(g)+ Y2(g) 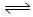 2XY(g);△H<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,图中对此过程的分析正确的是()
2XY(g);△H<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,图中对此过程的分析正确的是()
| A.图I是加入适当催化剂的变化情况 |
| B.图Ⅱ是扩大容器体积的变化情况 |
| C.图Ⅲ是增大压强的变化情况 |
| D.图Ⅲ是升高温度的变化情况 |