2012年"世界水日"的宣传主题是"水与粮食安全",水与生活生产有着密切关系,但今年1月15日,广西龙江河河段检测出重金属镉含量超标,严重威胁沿岸及下游居民饮水的安全。
(1)镉元素在元素周期表中的相关信息如图A,它的相对原子质量为

(2)富含蛋白质的食物可有效缓解重金属中毒症状,下列物质可缓解镉中毒的是
①玉米粥 ②食盐水 ③牛奶 ④西红柿 ⑤鸡蛋清 ⑥蔗糖水
(3)饮用酸碱度过大的水不利于人体健康.测定水样的酸碱度可用
(4)电解水时,电能转化成
下图是家用豆浆机,请根据图回答下列问题: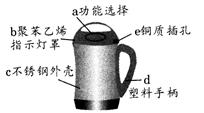
(1)制作材料中属于金属材料的是,(填一种)
(2)属于合成材料的是(选填一种物质编号),
(3)传统的生豆浆是用石磨来打磨的,打磨的过程是变化,
(4)用操作将黄豆渣分离的方法类似于我们实验中的操作,
(5)该豆浆机不能接触酸性物质,请用化学方程式解释
平静呼吸时,一般成年人每次吸入和呼出的气体量相等,约为500ml.气体成分测定和分析表明:吸入气、呼出气中各种气体成分的百分比大致如下表所示:
| 气体成分% |
氮气 |
氧气 |
二氧化碳 |
水蒸气 |
其它 |
| 吸入气体% |
78 |
21 |
0.03 |
0.01 |
0.96 |
| 呼出气体% |
78 |
16.4 |
4.63 |
0.03 |
0.94 |
(1).请根据在“我们吸入的空气和呼出的气体有什么不同”的活动与探究内容,填写下表
| 探究目的 |
实验操作 |
实验现象 |
得出结论 |
| 比较空气与呼出气体 中含二氧化碳气体的多少 |
取一瓶空气,一瓶呼出的气体,各滴入澄清的石灰水,振荡 |
||
| 空气中氧气的含量比呼出气体中的多 |
|||
| 被呼气的干燥玻璃片变的得模糊,玻璃片上有一层水雾,放置在空气中的玻璃片没有水雾出现 |
(2).试列举生活中事实证明下列结论.
| 生活中事例 |
结论 |
| 空气中含有氧气 |
|
| 空气中含有水蒸气 |
指出下列图示操作中的错误,并说明错误操作将引起的后果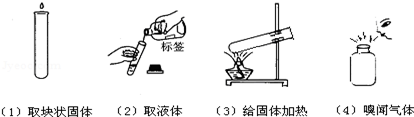
(1) _______;(2) ______ ___ ;
(3) _________;(4) _____ ____ 可能吸入有毒气体
根据下图所示仪器回答: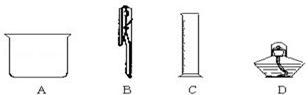
(1)写出仪器名称:
| A.______ ___ | B.___ ______ | C.____ _____ | D.____ _____ |
(2)填写仪器编号回答下列问题:
①配制溶液时,用来溶解固体的容器是 _____;②用于作热源的仪器是 ____;
③加热试管内溶液时,用于夹持试管的仪器是 _________ ;
④用来量度液体体积的是 _____用量筒量取液体时,读数时应 _______视;如果读数时采用俯视的方法,则读数结果会 ______(填“偏大”、“偏小”或“无影响”).
用托盘天平称量一个未知质量的烧杯,现用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减少砝码.请用“↑”和“↓”在下表中表示你的称量过程,并在图中用“‖”表示游码在标尺上的位置(假若烧杯的实际质量为36.8g).
| 砝码/g |
50 |
20 |
20 |
10 |
5 |
| 取用情况 |