在一定温度下,反应A2(g)+B2(g)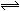 2AB(g),达到平衡的标志的是( )
2AB(g),达到平衡的标志的是( )
| A.容器内气体的总压强不随时间的变化而变化 |
| B.单位时间内有n mol A2生成,同时就有n mol B2生成 |
| C.单位时间内有n mol A2消耗,同时就有2n mol AB生成 |
| D.单位时间内有n mol B2发生反应,同时就有2n mol AB分解 |
分子式为C5H12的烃,其分子内含3个甲基,该烃的二氯代物的同分异构体的数目为
| A.8种 | B.9种 | C.10种 | D.11种 |
银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是
| A.处理过程中银器一直保持恒重 |
| B.银器为正极,Ag2S被还原生成单质银 |
| C.该过程中总反应为2Al+3Ag2S═6Ag+Al2S3 |
| D.黑色褪去的原因是黑色Ag2S转化为白色AgCl |
物质的量浓度相同的下列物质中,含粒子种类最多的是
| A.CaCl2 | B.CH3COONa | C.K2S | D.NH3 |
下列说法正确的是
| A.强电解质的水溶液中不存在溶质分子,弱电解质的水溶液中存在溶质分子和离子 |
| B.强电解质的水溶液导电性强于弱电解质的水溶液 |
| C.强电解质都是离子化合物,弱电解质都是共价化合物 |
| D.强电解质易溶于水,弱电解质难溶于水 |
已知温度T时水的离子积常数为 。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.a=b |
| B.混合溶液的pH=7 |
C.混合溶液中, |
D.混合溶液中, |