用NA表示阿伏伽德罗常数,下列说法中正确的是
| A.2.4g金属镁变成镁离子时失去的电子数为0.1NA |
| B.2g氢气中含有的原子数为2NA |
| C.标准状况下,22.4L水中含有的原子数目为1.5 NA |
| D.3.01×1023个氮分子中含有的原子数为2 NA |
下列实验不能达到目的的是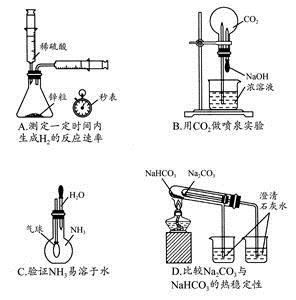
下列实验对应的结论不正确的是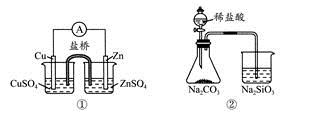
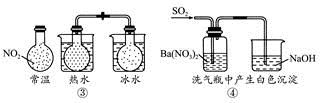
| A.①能组成Zn-Cu原电池 |
| B.②能证明非金属性Cl>C>Si |
C.③说明反应2NO2(g) N2O4(g),ΔH<0 N2O4(g),ΔH<0 |
| D.④白色沉淀为BaSO4 |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案: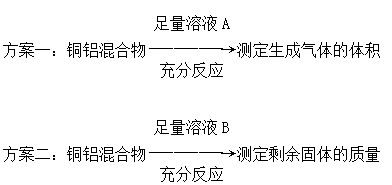
下列有关判断中不正确的是
| A.溶液A和溶液B均可以是盐酸或NaOH溶液 |
| B.若溶液B选用浓硝酸,测得铜的质量分数偏大 |
| C.方案一可能产生氢气,方案二可能剩余铜 |
| D.实验室中方案Ⅱ更便于实施 |
用试纸检验气体性质是一种重要的实验方法。如下图所示的实验中(可加热),下列试纸的选用、现象、对应结论都正确的一项是
| 选项 |
试剂B |
湿润的 试纸A |
现象 |
结论 |
| A |
碘水 |
淀粉试纸 |
变蓝 |
碘具有氧化性 |
| B |
浓氨水,生石灰 |
蓝色石蕊试纸 |
变红 |
氨气为碱性气体 |
| C |
Na2SO3,硫酸 |
品红试纸 |
褪色 |
SO2具有漂白性 |
| D |
Cu,浓硝酸 |
KI-淀粉 试纸 |
变蓝 |
NO2为 酸性气体 |
无论在化学实验室还是在家中进行实验或探究活动,都必须注意安全。下列实验操作正确的是
| A.用蒸发皿加热NaCl溶液 |
| B.不慎将汞滴落到桌面上,应立即用较多的水冲洗 |
| C.从试剂瓶中取出的一些Na2CO3溶液放入试管中,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| D.用瓷坩埚熔化氢氧化钠 |