在500mLFe2(SO4)3和CuSO4的混合溶液中加入16.8g的铁粉,搅拌并充分反应后,经过滤、洗涤、干燥,可得到6.4g铜。要使溶液中SO42-完全沉淀,需加入2.0mol·L-1的BaCl2溶液500mL。已知Fe3+的氧化性比Cu2+强,求:
(1)原溶液中SO42-离子的物质的量浓度。
(2)原混合溶液中硫酸铜的物质的量浓度。
氢气通常用生产水煤气的方法制得。其中CO(g)+ H2O(g) 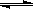 CO2(g)+ H2(g); △H<0。在850℃时,K=1。
CO2(g)+ H2(g); △H<0。在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K▲1(填“大于”、“小于”或“ 等于”)
等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入 1.0 mol CO、3.0molH2O、
1.0mol CO2和 x mol H2,则:
①当x=5.0时,上述平衡向▲(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是▲。
(3)在850℃时,若设x=5.0 mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a▲b(填“大于”、“小于”或“等于”)。
向一定量的Fe、FeO、Fe2O3混合物中加入1.00mol/l的盐酸100ml,可恰好使混合物完全溶解,放出224ml标准状况下的气体,向所得溶液中加入硫氰化钾,无血红色出现。
(1)若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量是多少?
(2)求原混合物中铁元素的质量分数 。
取一定量的Na2CO3、NaHCO3和Na2SO4混合物与250mL 1.00 mol·L-1过量盐酸反应,生成2.016L CO2(标准状况),然后加入500mL 0.100 mol·L-1 Ba(OH)2溶液,得到沉淀的质量为2.33g,溶液中过量的碱用10.0mL 1.00 mol·L-1盐酸恰好完全中和。计算混合物中各物质的质量。
如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,A池中混合液的体积为200 mL(电解前后体积视为不变),求通电前A池中原混合溶液Cu2+的浓度。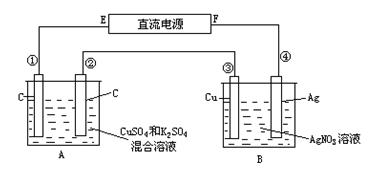
有一硝酸盐晶体,其化学式为M(NO3)x·yH2O,相对分子质量为242。取1.21g该晶体溶于水,配成100mL溶液,将此溶液用石墨作电极进行电解,当有0.01mol电子发生转移时,溶液中金属全部析出。经称量阴极增重0.32g。求:
(1)金属M的相对原子质量及x、y值。
(2)电解后溶液的pH(电解过程中溶液体积变化忽略不计)。