下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500ml的操作,请按要求填空:
(1)所需浓H2SO4的体积为
(2)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 (偏高、偏低、无影响)。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的 里,并不断搅拌,目的是 。
(4)将 的上述溶液沿 注入 中,并用50mL蒸馏水洗涤烧杯2~3次,洗涤液要 中,并摇匀。
(5)加水至距刻度 处,改用 加水,使溶液的凹液面正好跟刻度相平。
(15分)KMnO4是常用的强氧化剂,工业上以软锰矿(主要成分MnO2)为原料,通过液相法生产,即在碱性条件下用氧气氧化MnO2得到K2MnO4,分离后得到K2MnO4,再用惰性材料为电极电解K2MnO4溶液得到KMnO4,简略生产过程如下:
(1)反应器中反应的化学方程式为:。
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量最低的贫矿中Al、Si的氧化物含量较高,会导致KOH消耗量(填“偏高”或“偏低”),其中Al的氧化物和KOH溶液反应的化学方程式为:。
(3)电解槽中阳极的电极反应方程式为:;
(4)在传统工艺中得到K2MnO4后,向其中通入CO2制备KMnO4,化学反应方程式为:3K2MnO4+2CO2=2KMnO4+ MnO2+ 2K2CO3根据上述反应,从Mn元素的角度考虑KMnO4的产率最高为。与该传统工艺相比,电解法的优势是。
(5)测定高锰酸钾样品纯度的方法是:向高锰酸钾溶液中滴加硫酸锰溶液产生黑色沉淀,反应的离子方程式。
(6)已知常温下KSP﹝Mn(OH)2﹞=2.0×10-23,工业上调节PH沉淀废水中的Mn2+,当pH=10时,
c(Mn2+)= mol/L。
水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是__________。
(2)室温时,在由水电离产生的c(H+)=1×10-14 mol·L-1的溶液中,
①NH4+、Al3+、Br-、SO42-
②Na+、Mg2+、Cl-、NO3-
③K+、Ba2+、Cl-、NO3-
④K+、Na+、HCO3-、SO42-
四组离子中,一定可以大量共存的是_______(填序号,下同),可能大量共存的是_____________。
(3)在下列反应中属于氧化还原反应,水仅做氧化剂的是___________(填字母,下同),水既不做氧化剂又不做还原剂的是_______________。
A.CaO+H2O====Ca(OH)2
B.2Na2O2+2H2O====4NaOH+O2↑
C.2F2+2H2O====4HF+O2
D.3Fe+4H2O(g)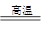 Fe3O4+4H2
Fe3O4+4H2
(4)已知铅蓄电池的反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O,
2PbSO4+2H2O,
①下列分析错误的是_____________。
A.铅蓄电池是最常用的可充电电池,在充电时,电池的正极应接直流电源的正极
B.铅蓄电池在放电时,电解液的酸性减弱
C.铅蓄电池在放电时,PbO2作为负极,不断转化为PbSO4
D.铅蓄电池在充电时,PbO2是氧化产物
②用该铅蓄电池电解1.8 mL水,电池内转移的电子数约为_________,消耗__________ mol硫酸。
(5)如图是某品牌饮用矿泉水标签的部分内容。
请认真阅读标签内容后计算。
①该矿泉水中镁离子的物质的量浓度的最大值是____;
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过___________mol。
有X、Y、Z三种元素,已知:
①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇KSCN溶液呈红色。
请回答下列问题:
(1)Y的最高价氧化物对应水化物的化学式是____________________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式____________。
此液体具有的性质是____________(填字母)。
| A.光束通过该液体时形成光亮的“通路” |
| B.插入电极通直流电后,有一极附近液体颜色加深 |
| C.向该液体中加入硝酸银溶液,无沉淀产生 |
| D.将该液体加热、蒸干、灼烧后,有氧化物生成 |
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,1 mol该气体被O2氧化放热98.0 kJ。若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率__________。
②原无色有刺激性气味的气体与含1.5 mol Y的含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应。可生成一种强酸和一种氧化物。若有1.5×6.02×1023个电子转移时,该反应的化学方程式是(用单线桥表示电子转移方向和数目):_____________________________________________。
(4)室温时,pH=5的HY溶液和pH=5的ZY3溶液中,水电离出的氢离子分别是mol·L-1和
mol·L-1
(12分)研究氮、硫元素的化合物具有重要意义。
(1)t0℃,p0kpa时,向固定容积为2L的密闭容器中充入2.0 mol SO2和1.0molO2,5分钟后达到平衡,测得生成1.0mol SO3(g),放出热量98.0kJ,则v(O2)=__________mol·L-1·min ,若继续通入2.0mol SO2和1.0mol O2,则平衡____________移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,__________mol<n(SO3)<__________mol。
,若继续通入2.0mol SO2和1.0mol O2,则平衡____________移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,__________mol<n(SO3)<__________mol。
已知t0℃,p0kpa时,N2和O2反应的能量变化如图所示:
则t0℃,P0kpa时,SO2与NO反应生成N2和SO3的热化学方程式为____________________。
(2)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生反应NO2(g)+SO2(g) 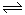 SO3(g)+NO(g),下列能说明反应达到平衡状态的是________(填写代号)。
SO3(g)+NO(g),下列能说明反应达到平衡状态的是________(填写代号)。
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO2和SO2的体积比保持不变
d.每消耗1mol SO3的同时生成1molNO2
测得上述反应平衡时NO2与SO2体积比为1:4,则平衡常数K=_____________。
(3)一定温度下,向氨水中加水稀释的过程中,NH3·H2O的电离程度______________(填“增大”、“减小”或“不变”,下同),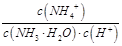 ________________。
________________。
(12分)电解池、原电池对于金属冶炼、实验室研究具有十分重要的意义。
(1)电解方法精炼粗铜,电解液选用CuSO4溶液,精炼过程中电解质溶液的浓度______________(填写“增大”、“减小”或“不变”)。铜在潮湿空气中会被锈蚀,写出该反应的化学方程式______________,锈蚀过程中发生了原电池反应,该电池的正极反应式为______________。
(2)研究发现有机合成反应可形成原电池,既生产产品,又生产电能。例如烯烃生产卤代烃的反应就可制成原电池,若电池总反应表示为:
则该原电池的负极反应式为_________________________。
(3)如图为Mg-NaClO燃料电池结构示意图,已知电解质溶液为NaOH溶液,且两电极中一个为石墨电极,一个为镁电极。
Y电极材料为_____________,X电极发生的电极反应式为_____________,若该电池开始时加入1L0.2 mol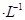 NaOH溶液,然后从下口充入1L 0.1mol
NaOH溶液,然后从下口充入1L 0.1mol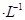 NaClO溶液(忽略整个过程的体积变化),当NaClO完全放电时溶液的pH=_______________。
NaClO溶液(忽略整个过程的体积变化),当NaClO完全放电时溶液的pH=_______________。